Cloruro de tionilo - Thionyl chloride

|
|

|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Dicloruro sulfuroso
|
|
| Otros nombres | |
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.028.863 |
| Número CE | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 1836 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| SOCl 2 | |
| Masa molar | 118,97 g / mol |
| Apariencia | Líquido incoloro (amarillea al envejecer) |
| Olor | Picante y desagradable |
| Densidad | 1.638 g / cm 3 , líquido |
| Punto de fusion | −104,5 ° C (−156,1 ° F; 168,7 K) |
| Punto de ebullición | 74,6 ° C (166,3 ° F; 347,8 K) |
| Reacciona | |
| Solubilidad | Soluble en la mayoría de disolventes apróticos: tolueno , cloroformo , éter dietílico . Reacciona con disolventes próticos como alcoholes. |
| Presión de vapor | |
|
Índice de refracción ( n D )
|
1.517 (20 ° C) |
| Viscosidad | 0,6 cP |
| Estructura | |
| piramidal | |
| 1,44 D | |
| Termoquímica | |
|
Capacidad calorífica ( C )
|
121,0 J / mol (líquido) |
|
Entropía molar estándar ( S |
309,8 kJ / mol (gas) |
| −245,6 kJ / mol (líquido) | |
| Riesgos | |
| Principales peligros | |
| Pictogramas GHS |
  
|
| Palabra de señal GHS | Peligro |
| H302 , H314 , H331 | |
| P261 , P280 , P305 + 351 + 338 , P310 | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | No es inflamable |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
Ninguno |
|
REL (recomendado)
|
C 1 ppm (5 mg / m 3 ) |
|
IDLH (peligro inmediato)
|
DAKOTA DEL NORTE |
| Compuestos relacionados | |
|
Haluros de tionilo relacionados
|
|
|
Compuestos relacionados
|
|
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El cloruro de tionilo es un compuesto inorgánico con la fórmula química S O Cl
2. Es un líquido incoloro moderadamente volátil con un olor acre desagradable. El cloruro de tionilo se utiliza principalmente como reactivo de cloración, produciéndose aproximadamente 45.000 toneladas (50.000 toneladas cortas) por año a principios de la década de 1990, pero ocasionalmente también se utiliza como disolvente. Es tóxico, reacciona con el agua y también está incluido en la Convención sobre Armas Químicas, ya que puede usarse para la producción de armas químicas .
El cloruro de tionilo a veces se confunde con el cloruro de sulfurilo , SO 2 Cl 2 , pero las propiedades de estos compuestos difieren significativamente. El cloruro de sulfurilo es una fuente de cloro, mientras que el cloruro de tionilo es una fuente de iones cloruro .
Producción
La principal síntesis industrial implica la reacción de trióxido de azufre y dicloruro de azufre : esta síntesis se puede adaptar al laboratorio calentando oleum para destilar lentamente el trióxido de azufre en un matraz enfriado de dicloruro de azufre.
- SO 3 + SCl 2 → SOCl 2 + SO 2
Otros métodos incluyen síntesis a partir de pentacloruro de fósforo , dicloruro de cloro y azufre o fosgeno :
- SO 2 + PCl 5 → SOCl 2 + POCl 3
- SO 2 + Cl 2 + SCl 2 → 2 SOCl 2
- SO 3 + Cl 2 + 2 SCl 2 → 3 SOCl 2
- SO 2 + COCl 2 → SOCl 2 + CO 2
La primera de las cuatro reacciones anteriores también produce oxicloruro de fósforo (cloruro de fosforilo), que se asemeja al cloruro de tionilo en muchas de sus reacciones.
Propiedades y estructura
SOCl 2 adopta una geometría molecular piramidal trigonal con simetría molecular C s . Esta geometría se atribuye a los efectos del par solitario en el centro central de azufre (IV).
En estado sólido, el SOCl 2 forma cristales monoclínicos con el grupo espacial P2 1 / c.
Estabilidad
El cloruro de tionilo tiene una vida útil prolongada, sin embargo, las muestras "envejecidas" desarrollan un tono amarillo, posiblemente debido a la formación de dicloruro de disulfuro . Se descompone lentamente en S 2 Cl 2 , SO 2 y Cl 2 justo por encima del punto de ebullición. El cloruro de tionilo es susceptible a la fotólisis, que procede principalmente a través de un mecanismo de radicales. Las muestras que presenten signos de envejecimiento pueden purificarse mediante destilación a presión reducida para obtener un líquido incoloro.
Reacciones
El cloruro de tionilo se utiliza principalmente en la producción industrial de compuestos organoclorados , que a menudo son productos intermedios en productos farmacéuticos y agroquímicos. Suele preferirse a otros reactivos, como el pentacloruro de fósforo , ya que sus subproductos (HCl y SO 2 ) son gaseosos, lo que simplifica la purificación del producto.
Muchos de los productos del cloruro de tionilo son en sí mismos altamente reactivos y, como tales, participan en una amplia gama de reacciones.
Con agua y alcoholes
El cloruro de tionilo reacciona exotérmicamente con agua para formar dióxido de azufre y ácido clorhídrico :
- SOCl 2 + H 2 O → 2 HCl + SO 2
Mediante un proceso similar, también reacciona con alcoholes para formar cloruros de alquilo . Si el alcohol es quiral la reacción transcurre generalmente a través de una S N i mecanismo con retención de la estereoquímica; sin embargo, dependiendo de las condiciones exactas empleadas, también se puede lograr la estéreoinversión. Históricamente, el uso de SOCl 2 en combinación con una amina terciaria como la piridina se denominaba halogenación de Darzens , pero los químicos modernos rara vez utilizan este nombre.
Las reacciones con un exceso de alcohol producen ésteres de sulfito , que pueden ser potentes reactivos de metilación , alquilación e hidroxialquilación.
- SOCl 2 + 2 ROH → (RO) 2 SO + 2 HCl
Por ejemplo, la adición de SOCl 2 a aminoácidos en metanol produce selectivamente los correspondientes ésteres metílicos.
Con ácidos carboxílicos
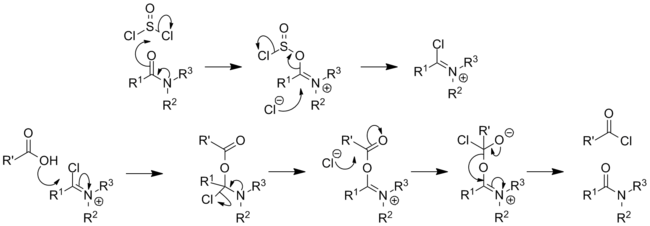
Clásicamente, convierte los ácidos carboxílicos en cloruros de acilo :
- SOCl 2 + RCO 2 H → RCOCl + SO 2 + HCl
Se ha investigado el mecanismo de reacción:
Con especies de nitrógeno
Con las aminas primarias, el cloruro de tionilo da derivados de sulfinilamina (RNSO), siendo un ejemplo la N - sulfinilanilina . El cloruro de tionilo reacciona con formamidas primarias para formar isocianuros y con formamidas secundarias para dar iones de cloro iminio ; ya que tal reacción con dimetilformamida formará el reactivo de Vilsmeier . Mediante un proceso análogo, las amidas primarias reaccionarán con el cloruro de tionilo para formar cloruros de imidoílo , y las amidas secundarias también darán iones de cloro iminio . Estas especies son altamente reactivas y pueden usarse para catalizar la conversión de ácidos carboxílicos en cloruros de acilo, también se aprovechan en la reacción de Bischler-Napieralski como medio para formar isoquinolinas .
Las amidas primarias continuarán formando nitrilos si se calientan ( degradación de amida de Von Braun ). El cloruro de tionilo también se ha utilizado para promover la transposición de las oximas de Beckmann .
Con especies de azufre
- El cloruro de tionilo transformará los ácidos sulfínicos en cloruros de sulfinilo
- Los ácidos sulfónicos reaccionan con cloruro de tionilo para producir cloruros de sulfonilo . También se han preparado cloruros de sulfonilo a partir de la reacción directa de la sal de diazonio correspondiente con cloruro de tionilo.
- El cloruro de tionilo se puede utilizar en variaciones de la transposición de Pummerer .
Con especies de fósforo
El cloruro de tionilo convierte los ácidos fosfónicos y fosfonatos en cloruros de fosforilo . Es por este tipo de reacción que el cloruro de tionilo se enumera como la Lista 3 compuesto, ya que se puede utilizar en el método de "di-di" de la producción de la serie G agentes nerviosos . Por ejemplo, el cloruro de tionilo convierte el metilfosfonato de dimetilo en dicloruro de ácido metilfosfónico , que se puede utilizar en la producción de sarín y somán .
Con metales
Como SOCl 2 reacciona con el agua se puede utilizar para deshidratar diversos hidratos de cloruro de metal, tal MgCl 2 · 6H 2 O , AlCl 3 · 6H 2 O , y FeCl 3 · 6H 2 O . Esta conversión implica el tratamiento con cloruro de tionilo a reflujo y sigue la siguiente ecuación general:
- MCl n · x H 2 O + x SOCl 2 → MCl n + x SO 2 + 2 x HCl
Otras reacciones
- El cloruro de tionilo puede participar en una variedad de reacciones de adición electrofílica diferentes. Se agrega a los alquenos en presencia de AlCl 3 para formar un complejo de aluminio que puede hidrolizarse para formar un ácido sulfínico. Tanto los cloruros de aril sulfinilo como los diaril sulfóxidos se pueden preparar a partir de arenos mediante la reacción con cloruro de tionilo en ácido tríflico o la presencia de catalizadores tales como BiCl 3 , Bi (OTf) 3 , LiClO 4 o NaClO 4 .
- En el laboratorio, se puede utilizar una reacción entre el cloruro de tionilo y un exceso de alcohol anhidro para producir soluciones alcohólicas anhidras de HCl .
- El cloruro de tionilo se somete a reacciones de intercambio de halógenos para dar compuestos como bromuro de tionilo y fluoruro de tionilo.
Pilas
Cloruro de tionilo es un componente de cloruro de litio-tionilo baterías , donde actúa como el electrodo positivo ( ánodo ) con litio que forma el electrodo negativo ( cátodo ); el electrolito es típicamente tetracloroaluminato de litio . La reacción de descarga general es la siguiente:
- 4 Li + 2 SOCl 2 → 4 LiCl + S + SO 2
Estas baterías no recargables tienen muchas ventajas sobre otras formas de batería de litio, como una alta densidad de energía, un amplio rango de temperatura operativa y una larga vida útil operativa y de almacenamiento. Sin embargo, su alto costo y las preocupaciones de seguridad han limitado su uso. El contenido de las baterías es altamente tóxico y requiere procedimientos especiales de eliminación; además, pueden explotar si se cortocircuitan. La tecnología se utilizó en el rover Sojourner Mars.
La seguridad
El SOCl 2 es un compuesto reactivo que puede liberar violentamente gases peligrosos al entrar en contacto con agua y otros reactivos. También está controlado por la Convención de armas químicas y aparece como un 3 Horario sustancia ya que se utiliza en el método de "di-di" de la producción de la serie G agentes nerviosos .
Historia
En 1849, los químicos franceses Jean-François Persoz y Bloch, y el químico alemán Peter Kremers (1827-?), Sintetizaron por primera vez de forma independiente cloruro de tionilo haciendo reaccionar pentacloruro de fósforo con dióxido de azufre . Sin embargo, sus productos eran impuros: tanto Persoz como Kremers afirmaron que el cloruro de tionilo contenía fósforo, y Kremers registró su punto de ebullición en 100 ° C (en lugar de 74,6 ° C). En 1857, el químico germano-italiano Hugo Schiff sometió cloruro de tionilo crudo a destilaciones fraccionadas repetidas y obtuvo un líquido que hirvió a 82 ° C y que llamó cloruro de tionilo . En 1859, el químico alemán Georg Ludwig Carius señaló que el cloruro de tionilo podría usarse para fabricar anhídridos de ácido y cloruros de acilo a partir de ácidos carboxílicos y para fabricar cloruros de alquilo a partir de alcoholes .