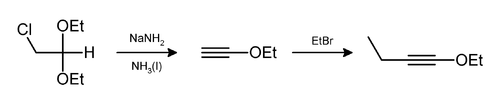Amida de sodio - Sodium amide

|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Amida de sodio, azanida de sodio
|
|
| Otros nombres
Sodamida
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.029.064 |
| Número CE | |
|
PubChem CID
|
|
| UNII | |
| un numero | 1390 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| NaNH 2 | |
| Masa molar | 39,01 g mol −1 |
| Apariencia | Cristales incoloros |
| Olor | similar al amoniaco |
| Densidad | 1,39 g cm −3 |
| Punto de fusion | 210 ° C (410 ° F; 483 K) |
| Punto de ebullición | 400 ° C (752 ° F; 673 K) |
| reacciona | |
| Solubilidad | 0,004 g / 100 mL (amoniaco líquido), reacciona en etanol |
| Acidez (p K a ) | 38 ( ácido conjugado ) |
| Estructura | |
| ortorrómbico | |
| Termoquímica | |
|
Capacidad calorífica ( C )
|
66,15 J / mol K |
|
Entropía molar estándar ( S |
76,9 J / mol K |
| -118,8 kJ / mol | |
|
Energía libre de Gibbs (Δ f G ˚)
|
-59 kJ / mol |
| Riesgos | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | 4,44 ° C (39,99 ° F; 277,59 K) |
| 450 ° C (842 ° F; 723 K) | |
| Compuestos relacionados | |
|
Otros aniones
|
Bis (trimetilsilil) amida de sodio |
|
Otros cationes
|
Amida de litio amida de potasio |
|
Compuestos relacionados
|
Amoníaco |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
La amida de sodio , comúnmente llamada sodamida (nombre sistemático azanida de sodio ), es el compuesto inorgánico con la fórmula NaNH 2 . Es una sal compuesta por el catión sodio y el anión azanida . Este sólido, que es peligrosamente reactivo con el agua, es blanco, pero las muestras comerciales suelen ser grises debido a la presencia de pequeñas cantidades de hierro metálico del proceso de fabricación. Estas impurezas no suelen afectar la utilidad del reactivo . El NaNH 2 conduce la electricidad en estado fusionado, siendo su conductancia similar a la del NaOH en un estado similar. El NaNH 2 se ha empleado ampliamente como una base fuerte en síntesis orgánica .
Preparación y estructura
La amida de sodio se puede preparar mediante la reacción de sodio con gas amoniaco, pero normalmente se prepara mediante la reacción en amoniaco líquido utilizando nitrato de hierro (III) como catalizador . La reacción es más rápida en el punto de ebullición del amoniaco, c. -33 ° C. Un electruro , [Na (NH 3 ) 6 ] + e - , se forma como un intermedio de reacción .
- 2 Na + 2 NH 3 → 2 NaNH 2 + H 2
El NaNH 2 es un material similar a la sal y, como tal, cristaliza como un polímero infinito. La geometría del sodio es tetraédrica. En el amoníaco, el NaNH 2 forma soluciones conductoras, en consonancia con la presencia de iones Na (NH 3 ) 6 + y NH 2 - .
Usos
La amida de sodio se usa principalmente como una base fuerte en química orgánica, a menudo en solución de amoníaco líquido. Es el reactivo de elección para el secado de amoniaco (líquido o gaseoso). Una de las principales ventajas del uso de amida de sodio es que funciona principalmente como nucleófilo . En la producción industrial de índigo , la amida de sodio es un componente de la mezcla altamente básica que induce la ciclación de N -fenilglicina . La reacción produce amoníaco, que normalmente se recicla.

Deshidrohalogenación
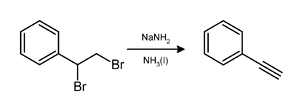
Amida de sodio induce la pérdida de dos equivalentes de bromuro de hidrógeno a partir de un vicinal dibromoalcano para dar un enlace carbono-carbono triples , como en una preparación de fenilacetileno . Normalmente, dos equivalentes de amida de sodio producen el alquino deseado. Se necesitan tres equivalentes en la preparación de alquinos terminales porque el CH terminal del alquino resultante protona una cantidad equivalente de base.
El cloruro de hidrógeno y el etanol también se pueden eliminar de esta manera, como en la preparación de 1-etoxi-1-butino.
Reacciones de ciclación
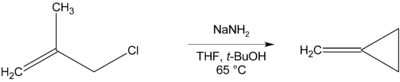
Cuando no hay β-hidrógeno que eliminar, se pueden formar compuestos cíclicos, como en la preparación de metilenciclopropano a continuación.
Los ciclopropenos , aziridinas y ciclobutanos pueden formarse de manera similar.
Desprotonación de ácidos de carbono y nitrógeno
Los ácidos de carbono que pueden ser desprotonados por amida sódica en amoniaco líquido incluyen alquinos terminales , metilcetonas , ciclohexanona , ácido fenilacético y sus derivados y difenilmetano . La acetilacetona pierde dos protones para formar un dianión . La amida de sodio también desprotona indol y piperidina .
Bases no nucleofílicas relacionadas
Sin embargo, es poco soluble en disolventes distintos del amoniaco. Su uso ha sido reemplazado por los reactivos relacionados hidruro de sodio , bis (trimetilsilil) amida de sodio (NaHMDS) y diisopropilamida de litio (LDA).
Otras reacciones
- Reordenamiento con ortodeprotonación
- Síntesis de oxirano
- Síntesis de indol
- Reacción de chichibabin
La seguridad
La amida de sodio reacciona violentamente con el agua para producir amoníaco e hidróxido de sodio y se quema en el aire para producir óxidos de sodio y dióxido de nitrógeno .
- NaNH 2 + H 2 O → NH 3 + NaOH
- 4 NaNH 2 + 7 O 2 → 2 Na 2 O + 4 NO 2 + 4 H 2 O
En presencia de cantidades limitadas de aire y humedad, como en un recipiente mal cerrado, se pueden formar mezclas explosivas de peróxidos. Esto va acompañado de un amarilleamiento o pardeamiento del sólido. Como tal, la amida de sodio debe almacenarse en un recipiente herméticamente cerrado, bajo una atmósfera de gas inerte. Las muestras de amida de sodio que son de color amarillo o marrón representan riesgos de explosión.