Piperidina - Piperidine
|
|
|||

|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
Piperidina |
|||
| Otros nombres
Hexahidropiridina
Azaciclohexano Pentametilenamina Azinane |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.003.467 |
||
| Número CE | |||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| un numero | 2401 | ||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 5 H 11 N | |||
| Masa molar | 85,150 g · mol −1 | ||
| Apariencia | Líquido incoloro | ||
| Olor | Similar al semen, a pescado-amoniacal, picante | ||
| Densidad | 0,862 g / ml | ||
| Punto de fusion | -7 ° C (19 ° F; 266 K) | ||
| Punto de ebullición | 106 ° C (223 ° F; 379 K) | ||
| Miscible | |||
| Acidez (p K a ) | 11.22 | ||
| -64,2 · 10 −6 cm 3 / mol | |||
| Viscosidad | 1.573 cP a 25 ° C | ||
| Riesgos | |||
| Ficha de datos de seguridad | MSDS1 , MSDS2 | ||
| Pictogramas GHS |
  
|
||
| Palabra de señal GHS | Peligro | ||
| H225 , H311 , H314 , H331 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P260 , P261 , P264 , P271 , P280 , P301 + 330 + 331 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P310 , P311 , P312 , P321 , P322 , P361 , P363 , P370 + 378 , P403 + 233 | |||
| NFPA 704 (diamante de fuego) | |||
| Compuestos relacionados | |||
|
Compuestos relacionados
|
La piridina pirrolidina piperazina Phosphorinane Arsinane |
||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
La piperidina es un compuesto orgánico con la fórmula molecular (CH 2 ) 5 NH. Esta amina heterocíclica consta de un anillo de seis miembros que contiene cinco puentes de metileno (–CH 2 -) y un puente de amina (–NH–). Es un líquido incoloro con un olor descrito como desagradable y típico de las aminas . El nombre proviene del nombre del género Piper , que es la palabra latina para pimienta . Aunque la piperidina es un compuesto orgánico común, es mejor conocida como un elemento de estructura representativo dentro de muchos productos farmacéuticos y alcaloides , como las solenopsinas naturales .
Producción
La piperidina fue reportada por primera vez en 1850 por el químico escocés Thomas Anderson y nuevamente, de forma independiente, en 1852 por el químico francés Auguste Cahours , quien la nombró. Ambos obtuvieron piperidina haciendo reaccionar piperina con ácido nítrico.
Industrialmente, la piperidina se produce mediante la hidrogenación de piridina , generalmente sobre un catalizador de disulfuro de molibdeno :
- C 5 H 5 N + 3 H 2 → C 5 H 10 NH
La piridina también se puede reducir a piperidina mediante una reducción de abedul modificada utilizando sodio en etanol .
Aparición natural de piperidina y derivados.
La propia piperidina se ha obtenido de la pimienta negra , de Psilocaulon absimile ( Aizoaceae ) y de Petrosimonia monandra .
El motivo estructural de la piperidina está presente en numerosos alcaloides naturales . Estos incluyen piperina , que le da a la pimienta negra su sabor picante. Esto le dio al compuesto su nombre. Otros ejemplos son la solenopsina de la toxina de la hormiga de fuego , el análogo de nicotina anabasina del tabaco de árbol ( Nicotiana glauca ), la lobelina del tabaco indio y el alcaloide tóxico coniína de la cicuta venenosa , que se utilizó para matar a Sócrates .
Conformación
La piperidina prefiere una conformación de silla , similar al ciclohexano . A diferencia del ciclohexano, la piperidina tiene dos conformaciones de silla distinguibles: una con el enlace N-H en una posición axial y la otra en una posición ecuatorial. Después de mucha controversia durante las décadas de 1950 y 1970, se descubrió que la conformación ecuatorial era más estable en 0,72 kcal / mol en la fase gaseosa. En solventes no polares , se ha estimado un rango entre 0.2 y 0.6 kcal / mol, pero en solventes polares el conformador axial puede ser más estable. Los dos confórmeros se interconvierten rápidamente a través de la inversión de nitrógeno ; la barrera de activación de energía libre para este proceso, estimada en 6,1 kcal / mol, es sustancialmente más baja que las 10,4 kcal / mol para la inversión de anillo . En el caso de la N -metilpiperidina, la conformación ecuatorial se prefiere en 3,16 kcal / mol, que es mucho mayor que la preferencia en el metilciclohexano , 1,74 kcal / mol.
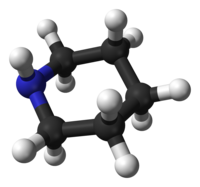 |

|
| conformación axial | conformación ecuatorial |
Reacciones
La piperidina se usa ampliamente para convertir cetonas en enaminas . Las enaminas derivadas de la piperidina son sustratos en la reacción de alquilación de enamina de Stork .
Tras el tratamiento con hipoclorito de calcio , la piperidina se convierte en N-cloropiperidina , una cloramina con la fórmula C 5 H 10 NCl. La cloramina resultante se somete a deshidrohalogenación para producir la imina cíclica.
Desplazamientos químicos de RMN
Usos
La piperidina se utiliza como disolvente y como base . Lo mismo es cierto para ciertos derivados: N -formilpiperidina es un solvente aprótico polar con mejor solubilidad en hidrocarburos que otros solventes amídicos , y la 2,2,6,6-tetrametilpiperidina es una base altamente estéricamente impedida , útil debido a su baja nucleofilia y alta solubilidad en disolventes orgánicos .
Una aplicación industrial importante de la piperidina es para la producción de tetrasulfuro de dipiperidinil ditiuram, que se utiliza como acelerador de la vulcanización del caucho con azufre .
Lista de medicamentos de piperidina
La piperidina y sus derivados son bloques de construcción ubicuos en productos farmacéuticos y químicos finos. La estructura de la piperidina se encuentra, por ejemplo, en:
- Icaridin (repelente de insectos)
- ISRS ( inhibidores selectivos de la recaptación de serotonina )
- estimulantes y nootrópicos :
- SERM ( moduladores selectivos del receptor de estrógeno )
- Vasodilatadores
- Medicamentos antipsicóticos :
-
Opioides :
- Dipipanona
- Fentanilo y análogos
- Loperamida
- Petidina (meperidina)
- Prodine
-
Arilciclohexilaminas :
- PCP y análogos
-
armas químicas anticolinérgicas
- Ditran
- Benzilato de N -metil-3-piperidilo (JB-336, BZ)
La piperidina también se usa comúnmente en reacciones de degradación química, como la secuenciación del ADN en la escisión de nucleótidos modificados particulares . La piperidina también se usa comúnmente como base para la desprotección de Fmoc , aminoácidos usados en la síntesis de péptidos en fase sólida .
La piperidina figura como un precursor de la Tabla II en la Convención de las Naciones Unidas contra el Tráfico Ilícito de Estupefacientes y Sustancias Psicotrópicas debido a su uso (que alcanzó su punto máximo en la década de 1970) en la fabricación clandestina de PCP (1- (1-fenilciclohexil) piperidina, también conocida como polvo de ángel, sherms, mojado, etc.).
Referencias
enlaces externos
-
 Medios relacionados con la piperidina en Wikimedia Commons
Medios relacionados con la piperidina en Wikimedia Commons



