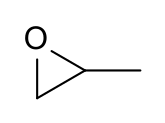
Óxido de propileno - Propylene oxide
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
(2R) -2-Metiloxirano (2S) -2-Metiloxirano |
|
| Otros nombres
El óxido de propileno
epoxipropano propileno epóxido de 1,2-propileno óxido de oxirano de metilo 1,2-epoxipropano propeno óxido de metilo óxido de etileno óxido de metiletileno |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.000.800 |
| Número CE | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 3 H 6 O | |
| Masa molar | 58.080 g · mol −1 |
| Apariencia | Líquido incoloro |
| Olor | similar al benceno |
| Densidad | 0,859 g / cm 3 |
| Punto de fusion | −111,9 ° C (−169,4 ° F; 161,2 K) |
| Punto de ebullición | 35 ° C (95 ° F; 308 K) |
| 41% (20 ° C) | |
| Presión de vapor | 445 mmHg (20 ° C) |
| −4,25 × 10 −5 cm 3 / mol | |
|
Índice de refracción ( n D )
|
1.3660 |
| Termoquímica | |
|
Capacidad calorífica ( C )
|
120,4 J · (K · mol) −1 |
|
Entropía molar estándar ( S |
196,5 J · (K · mol) −1 |
| −123,0 kJ · mol −1 | |
| Peligros | |
| Principales peligros | Extremadamente inflamable |
| Pictogramas GHS |
  
|
| Palabra de señal GHS | Peligro |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | -37 ° C (-35 ° F; 236 K) |
| 747 ° C (1.377 ° F; 1.020 K) | |
| Límites explosivos | 2,3–36% |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis media )
|
660 mg / kg (cobaya, oral) 380 mg / kg (rata, oral) 440 mg / kg (ratón, oral) 1140 mg / kg (rata, oral) 690 mg / kg (cobaya, oral) |
|
LC 50 ( concentración media )
|
1740 ppm (ratón, 4 h) 4000 ppm (rata, 4 h) |
|
LC Lo ( menor publicado )
|
2005 ppm (perro, 4 h) 4000 ppm (conejillo de indias, 4 h) |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
TWA 100 ppm (240 mg / m 3 ) |
|
REL (recomendado)
|
California |
|
IDLH (peligro inmediato)
|
Ca [400 ppm] |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El óxido de propileno es un compuesto orgánico con la fórmula molecular CH 3 CHCH 2 O. Este líquido volátil incoloro con un olor parecido al éter, se produce a gran escala industrialmente. Su principal aplicación es su uso para la producción de polioles de poliéter para su uso en la fabricación de plásticos de poliuretano . Es un epóxido quiral , aunque se usa comúnmente como mezcla racémica .
Este compuesto a veces se denomina óxido de 1,2-propileno para distinguirlo de su isómero óxido de 1,3-propileno, más conocido como oxetano .
Producción
La producción industrial de óxido de propileno comienza a partir de propileno . Se emplean dos enfoques generales, uno que implica hidrocloración y otro que implica oxidación. En 2005, aproximadamente la mitad de la producción mundial se realizó a través de la tecnología de la clorhidrina y la otra mitad a través de rutas de oxidación. Este último enfoque está adquiriendo una importancia cada vez mayor.
Vía de hidrocloración
La ruta tradicional procede a través de la conversión de propeno en propileno clorhidrina de acuerdo con el siguiente esquema simplificado:
A continuación, se deshidroclora la mezcla de 1-cloro-2-propanol y 2-cloro-1-propanol. Por ejemplo:
La cal ( hidróxido de calcio ) se usa a menudo para absorber el HCl .
Oxidación de propileno
La otra ruta general al óxido de propileno implica la oxidación del propileno con un peróxido orgánico. La reacción sigue esta estequiometría:
- CH 3 CH = CH 2 + RO 2 H → CH 3 CHCH 2 O + ROH
El proceso se practica con cuatro hidroperóxidos :
- En el proceso Halcon , el hidroperóxido de t- butilo se deriva de la oxigenación del isobutano , que produce t -butanol . Este coproducto se puede deshidratar a isobuteno, convertido en MTBE , un aditivo para gasolina .
- Hidroperóxido de etilbenceno , derivado de la oxigenación del etilbenceno , que produce 1-feniletanol. Este coproducto se puede deshidratar para dar estireno , un monómero útil.
- Hidroperóxido de cumeno derivado de la oxigenación de cumeno (isopropilbenceno), que produce alcohol cumílico. Mediante deshidratación e hidrogenación, este coproducto se puede reciclar de nuevo a cumeno. Esta tecnología fue comercializada por Sumitomo Chemical.
- El peróxido de hidrógeno es el oxidante en el proceso de peróxido de hidrógeno a óxido de propileno (HPPO), catalizado por una silicalita dopada con titanio :
- C 3 H 6 + H 2 O 2 → C 3 H 6 O + H 2 O
En principio, este proceso produce sólo agua era un subproducto. En la práctica, se generan algunas derivadas de PO de anillo abierto.
Reacciones
Como otros epóxidos, el PO sufre reacciones de apertura de anillo. Con agua se produce propilenglicol. Con los alcoholes, ocurren reacciones, llamadas hidroxilpropilación , análogas a la etoxilación . Los reactivos de Grignard se agregan al óxido de propileno para dar alcoholes secundarios.
Algunas otras reacciones del óxido de propileno incluyen:
- La reacción con óxido de aluminio a 250-260 ° C produce propionaldehído y un poco de acetona .
- La reacción con óxido de plata (I) conduce a ácido acético .
- La reacción con la amalgama de sodio-mercurio y agua produce isopropanol .
Usos
Entre el 60 y el 70% de todo el óxido de propileno se convierte en poliéter polioles mediante el proceso llamado alcoxilación . Estos polioles son componentes básicos en la producción de plásticos de poliuretano . Aproximadamente el 20% del óxido de propileno se hidroliza en propilenglicol , mediante un proceso que se acelera mediante catálisis ácida o básica . Otros productos importantes son polipropilenglicol , éteres de propilenglicol y carbonato de propileno .
Usos de nicho
Fumigante
La Administración de Drogas y Alimentos de los Estados Unidos aprobó el uso de óxido de propileno para pasteurizar almendras crudas a partir del 1 de septiembre de 2007, en respuesta a dos incidentes de contaminación por Salmonella en huertos comerciales, uno en Canadá y otro en los Estados Unidos. Las nueces de pistacho también se pueden someter a óxido de propileno para controlar la Salmonella .
Microscopía
El óxido de propileno se usa comúnmente en la preparación de muestras biológicas para microscopía electrónica , para eliminar el etanol residual usado previamente para la deshidratación. En un procedimiento típico, la muestra se sumerge primero en una mezcla de volúmenes iguales de etanol y óxido de propileno durante 5 minutos, y luego cuatro veces en óxido puro, 10 minutos cada una.
Seguridad
Es un carcinógeno humano potencial y está incluido en la Lista de carcinógenos del Grupo 2B de la IARC .
Ocurrencia natural
En 2016 se informó que se detectó óxido de propileno en Sagittarius B2 , una nube de gas en la Vía Láctea que pesa tres millones de masas solares . Es la primera molécula quiral detectada en el espacio, aunque sin exceso enantiomérico.
Referencias
Fuentes citadas
- Haynes, William M., ed. (2011). Manual CRC de Química y Física (92ª ed.). Boca Raton, FL: CRC Press . ISBN 1439855110.
enlaces externos
- Página de WebBook para C3H6O
- Óxido de propileno en la Agencia de Protección Ambiental de los Estados Unidos
- Óxido de propileno - información del producto químico: propiedades, producción, aplicaciones.
- Óxido de propileno en el sitio web de Technology Transfer Network Air Toxics
- CDC - Guía de bolsillo de NIOSH sobre peligros químicos

