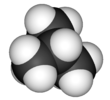
Isobutano - Isobutane
|
|
|||
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
2-metilpropano |
|||
| Otros nombres
Isobutano, R600a
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 1730720 | |||
| CHEBI | |||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.000.780 |
||
| Número CE | |||
| Número e | E943b (agentes de glaseado, ...) | ||
| 1301 | |||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| un numero | 1969 | ||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 4 H 10 | |||
| Masa molar | 58,124 g · mol −1 | ||
| Apariencia | Gas incoloro | ||
| Olor | Inodoro | ||
| Densidad | |||
| Punto de fusion | −159,42 ° C (−254,96 ° F; 113,73 K) | ||
| Punto de ebullición | −11,7 ° C (10,9 ° F; 261,4 K) | ||
| 48,9 mg⋅L −1 (a 25 ° C (77 ° F)) | |||
| Presión de vapor | 3,1 atm (310 kPa) (a 21 ° C (294 K; 70 ° F)) | ||
|
Constante de la ley de Henry ( k H ) |
8,6 nmol⋅Pa −1 ⋅kg −1 | ||
| Ácido conjugado | Isobutanio | ||
| −51,7 · 10 −6 cm 3 / mol | |||
| Termoquímica | |||
|
Capacidad calorífica ( C )
|
96,65 j⋅k -1 ⋅mol -1 | ||
| −134,8 - −133,6 kJ⋅mol −1 | |||
| −2,86959 - −2,86841 MJ⋅mol −1 | |||
| Peligros | |||
| Ficha de datos de seguridad |
Ver: página de datos lindeus.com |
||
| Pictogramas GHS |

|
||
| Palabra de señal GHS | Peligro | ||
| H220 | |||
| P210 | |||
| NFPA 704 (diamante de fuego) | |||
| punto de inflamabilidad | −83 ° C (−117 ° F; 190 K) | ||
| 460 ° C (860 ° F; 733 K) | |||
| Límites explosivos | 1,4–8,3% | ||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
|
PEL (permitido)
|
Ninguno | ||
|
REL (recomendado)
|
TWA 800 ppm (1900 mg / m 3 ) | ||
|
IDLH (peligro inmediato)
|
DAKOTA DEL NORTE | ||
| Compuestos relacionados | |||
|
Alcanos relacionados
|
Isopentano | ||
| Página de datos complementarios | |||
|
Índice de refracción ( n ), constante dieléctrica (ε r ), etc. |
|||
|
Datos termodinámicos |
Comportamiento de fase sólido-líquido-gas |
||
| UV , IR , RMN , MS | |||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El isobutano , también conocido como i- butano , 2-metilpropano o metilpropano , es un compuesto químico con fórmula molecular HC (CH 3 ) 3 . Es un isómero del butano . El isobutano es un gas incoloro e inodoro. Es el alcano más simple con un átomo de carbono terciario . El isobutano se utiliza como molécula precursora en la industria petroquímica , por ejemplo en la síntesis de isooctano .
Producción
El isobutano se obtiene por isomerización de butano .
Usos
El isobutano es la principal materia prima en las unidades de alquilación de las refinerías. Usando isobutano, se generan "mezclas de materiales" de grado gasolina con alta ramificación para buenas características de combustión. Los productos típicos de isobutano son 2,4-dimetilpentano y especialmente 2,2,4-trimetilpentano .
Solvente
En el proceso de lechada de Chevron Phillips para fabricar polietileno de alta densidad , se usa isobutano como diluyente. A medida que se elimina el polietileno en suspensión, el isobutano se evapora rápidamente, se condensa y se recicla de nuevo al reactor de bucle para este propósito.
Precursor del hidroperóxido de terc- butilo
El isobutano se oxida a hidroperóxido de terc- butilo , que posteriormente se hace reaccionar con propileno para producir óxido de propileno . El terc-butanol que resulta como subproducto se usa típicamente para fabricar aditivos de gasolina como el metil terc-butil éter (MTBE).
Usos varios
El isobutano también se utiliza como propulsor para latas de aerosol .
El isobutano se usa como parte de los combustibles mezclados, especialmente común en los botes de combustible que se usan para acampar .
Refrigerante
El isobutano se utiliza como refrigerante . El uso en refrigeradores comenzó en 1993 cuando Greenpeace presentó el proyecto Greenfreeze con la antigua empresa de Alemania Oriental Foron . En este sentido, las mezclas de "isobutano" puro y seco (R-600a) (es decir, mezclas de isobutano) tienen un potencial de agotamiento del ozono insignificante y un potencial de calentamiento global muy bajo (con un valor de 3,3 veces el GWP del dióxido de carbono) y pueden sirven como un reemplazo funcional para R-12 , R-22 (ambos son comúnmente conocidos por la marca registrada Freon ), R-134a y otros refrigerantes clorofluorocarbonados o hidrofluorocarbonados en sistemas convencionales de refrigeración y aire acondicionado estacionarios.
Como refrigerante, el isobutano presenta un riesgo de incendio y explosión además de los peligros asociados con los refrigerantes CFC no inflamables. La sustitución de este refrigerante por sistemas de aire acondicionado de vehículos de motor no diseñados originalmente para isobutano está ampliamente prohibida o desaconsejada.
Los vendedores y defensores de los refrigerantes de hidrocarburos argumentan en contra de tales prohibiciones con el argumento de que ha habido muy pocos incidentes de este tipo en relación con la cantidad de sistemas de aire acondicionado de vehículos llenos de hidrocarburos.
Nomenclatura
El nombre tradicional isobutano todavía se mantuvo en las recomendaciones de la IUPAC de 1993 , pero ya no se recomienda de acuerdo con las recomendaciones de 2013. Dado que la cadena continua más larga en isobutano contiene sólo tres átomos de carbono, el nombre IUPAC preferido es 2-metilpropano pero el localizador (2-) se omite típicamente en la nomenclatura general como redundante; C2 es la única posición en una cadena de propano donde se puede ubicar un sustituyente metilo sin alterar la cadena principal y formar el isómero constitucional n -butano.