Propeno - Propene
|
|
|||
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
Propeno |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.003.693 |
||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| un numero |
1077 En gas licuado de petróleo : 1075 |
||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 3 H 6 | |||
| Masa molar | 42.081 g · mol −1 | ||
| Apariencia | Gas incoloro | ||
| Densidad | 1,81 kg / m 3 , gas (1,013 bar, 15 ° C) 1,745 kg / m 3 , gas (1,013 bar, 25 ° C) 613,9 kg / m 3 , líquido |
||
| Punto de fusion | −185,2 ° C (−301,4 ° F; 88,0 K) | ||
| Punto de ebullición | −47,6 ° C (−53,7 ° F; 225,6 K) | ||
| 0,61 g / m 3 | |||
| -31,5 · 10 −6 cm 3 / mol | |||
| Viscosidad | 8,34 µPa · sa 16,7 ° C | ||
| Estructura | |||
| 0,366 D (gas) | |||
| Riesgos | |||
| Ficha de datos de seguridad | MSDS externa | ||
  
|
|||
| Frases R (desactualizadas) | 12 | ||
| Frases S (desactualizadas) | 16/9/33 | ||
| NFPA 704 (diamante de fuego) | |||
| punto de inflamabilidad | −108 ° C (−162 ° F; 165 K) | ||
| Compuestos relacionados | |||
|
Alquenos relacionados ;
grupos relacionados |
Etileno , isómeros de butileno ; Alilo , propenilo |
||
|
Compuestos relacionados
|
Propano , Propyne Propadiene , 1-Propanol 2-Propanol |
||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
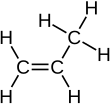
El propeno , también conocido como propileno , es un compuesto orgánico insaturado con la fórmula química . Tiene un doble enlace y es el segundo miembro más simple de la clase de hidrocarburos alquenos . Es un gas incoloro con un leve olor a petróleo.
Producción
Agrietamiento por vapor
La tecnología dominante para producir propileno es el craqueo al vapor. La misma tecnología se aplica al etano al etileno. Estas dos conversiones son los procesos n. ° 2 y n. ° 1 en la industria química, a juzgar por su escala. En este proceso, el propano se deshidrogena . El subproducto es hidrógeno:
- CH 3 CH 2 CH 3 → CH 3 CH = CH 2 + H 2
El rendimiento de propeno es aproximadamente del 85 % en m . Los subproductos se utilizan generalmente como combustible para la reacción de deshidrogenación del propano. El craqueo al vapor es uno de los procesos industriales que más energía consume.
La materia prima es nafta o propano , especialmente en el Medio Oriente , donde hay abundancia de propano de las operaciones de petróleo / gas. El propeno puede separarse mediante destilación fraccionada de mezclas de hidrocarburos obtenidas del craqueo y otros procesos de refinado; El propeno de grado de refinería es aproximadamente del 50 al 70%. En los Estados Unidos, el gas de esquisto es una fuente importante de propano.
Tecnología de conversión de olefinas
En la tecnología de conversión de triolefinas u olefinas de Phillips , el propileno se interconvierte con etileno y 2-butenos . Se utilizan catalizadores de renio y molibdeno :
- CH 2 = CH 2 + CH 3 CH = CHCH 3 → 2 CH 2 = CHCH 3
La tecnología se basa en una reacción de metátesis de olefinas descubierta en Phillips Petroleum Company . Se alcanzan rendimientos de propeno de aproximadamente 90% en peso.
Relacionado está el proceso de metanol a olefinas / metanol a propeno . Convierte el gas de síntesis (gas de síntesis) en metanol y luego convierte el metanol en etileno y / o propeno . El proceso produce agua como subproducto. El gas de síntesis se produce a partir de la reformación de gas natural o mediante la reformación inducida por vapor de productos del petróleo como la nafta, o mediante la gasificación del carbón .
Craqueo catalítico fluido
El craqueo catalítico de fluidos de alta severidad (FCC) utiliza la tecnología FCC tradicional en condiciones severas (relaciones de catalizador a aceite más altas, tasas de inyección de vapor más altas, temperaturas más altas, etc.) para maximizar la cantidad de propeno y otros productos ligeros. Una unidad de FCC de alta severidad generalmente se alimenta con gasóleos (parafinas) y residuos, y produce aproximadamente 20-25 m% de propeno en la materia prima junto con mayores volúmenes de gasolina de motor y subproductos destilados. Estos procesos de alta temperatura son costosos y tienen una gran huella de carbono. Por estas razones, las rutas alternativas al propileno continúan atrayendo la atención.
Investigación y mercado
La producción de propeno se ha mantenido estática en alrededor de 35 millones de toneladas (solo Europa y América del Norte) entre 2000 y 2008, pero ha ido en aumento en Asia oriental, sobre todo en Singapur y China. La producción mundial total de propeno es actualmente aproximadamente la mitad de la de etileno.
Se ha explorado el uso de enzimas modificadas genéticamente, pero no tiene valor comercial.
Usos
El propeno es el segundo producto de partida más importante en la industria petroquímica después del etileno . Es la materia prima de una amplia variedad de productos. Los fabricantes de polipropileno consumen casi dos tercios de la producción mundial. Los usos finales del polipropileno incluyen películas, fibras, envases, embalajes y tapas y cierres. El propeno también se utiliza para la producción de sustancias químicas importantes como el óxido de propileno, acrilonitrilo, cumeno, butiraldehído y ácido acrílico. En el año 2013 se procesaron alrededor de 85 millones de toneladas de propeno en todo el mundo.
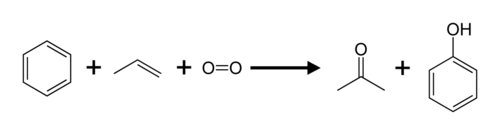
El propeno y el benceno se convierten en acetona y fenol mediante el proceso de cumeno .
El propeno también se usa para producir isopropanol (propan-2-ol), acrilonitrilo , óxido de propileno y epiclorhidrina . La producción industrial de ácido acrílico implica la oxidación catalítica parcial del propeno. El propeno también es un intermedio en la oxidación selectiva de propano en un solo paso a ácido acrílico. En la industria y los talleres, el propeno se utiliza como combustible alternativo al acetileno en la soldadura y corte con oxicombustible , soldadura fuerte y calentamiento de metales con el fin de doblarlos. Se ha convertido en un estándar en los productos BernzOmatic y otros en sustitutos de MAPP, ahora que el verdadero gas MAPP ya no está disponible.
Reacciones
El propeno se parece a otros alquenos en que sufre reacciones de adición con relativa facilidad a temperatura ambiente. La relativa debilidad de su doble enlace explica su tendencia a reaccionar con sustancias que pueden lograr esta transformación. Las reacciones de los alquenos incluyen: 1) polimerización , 2) oxidación , 3) halogenación e hidrohalogenación , 4) alquilación , 5) hidratación , 6) oligomerización y 7) hidroformilación .
Complejos de metales de transición
Los complejos de metal-propileno son fundamentales para la hidroformilación, la metátesis de alquenos y la polimerización , que son intermedios en estos procesos. El propileno es proquiral , lo que significa que la unión de un reactivo (como un electrófilo metálico) al grupo C = C produce uno de dos enantiómeros .
Polimerización
La mayor parte del propeno se utiliza para formar polipropileno, un termoplástico básico muy importante , a través de la polimerización por crecimiento de cadena . En presencia de un catalizador adecuado (típicamente un catalizador Ziegler-Natta ), el propeno polimerizará. Hay varias formas de lograr esto, como usar altas presiones para suspender el catalizador en una solución de propeno líquido o hacer pasar propeno gaseoso a través de un reactor de lecho fluidizado .
Combustión
El propeno se quema de manera similar a otros alquenos . En presencia de oxígeno suficiente o en exceso, el propeno se quema para formar agua y dióxido de carbono .
- 2 C 3 H 6 + 9 O 2 → 6 CO 2 + 6 H 2 O
La seguridad ambiental
El propeno es un producto de la combustión de los incendios forestales, el humo de los cigarrillos y los gases de escape de los vehículos de motor y los aviones. Es una impureza en algunos gases de calefacción. Las concentraciones observadas han estado en el rango de 0.1 a 4.8 partes por billón ( ppb ) en el aire rural, 4-10.5 ppb en el aire urbano y 7-260 ppb en muestras de aire industrial.
En los Estados Unidos y algunos países europeos se estableció un valor límite de 500 partes por millón ( ppm ) para la exposición ocupacional ( promedio ponderado en el tiempo de 8 horas ). Se considera un compuesto orgánico volátil (COV) y las emisiones están reguladas por muchos gobiernos, pero la Agencia de Protección Ambiental de los EE. UU. (EPA) no lo enumera como un contaminante peligroso del aire según la Ley de Aire Limpio . Con una vida media relativamente corta, no se espera que se bioacumule.
El propeno tiene una baja toxicidad aguda por inhalación y no se considera carcinógeno. Los estudios de toxicidad crónica en ratones no arrojaron evidencia significativa que sugiriera efectos adversos. Los seres humanos expuestos brevemente a 4.000 ppm no experimentaron ningún efecto perceptible. El propeno es peligroso por su potencial para desplazar el oxígeno como gas asfixiante y por su alto riesgo de inflamabilidad / explosión.
El biopropileno es el propileno de base biológica . Se ha examinado, motivado por diversos intereses como la huella de carbono . Se ha considerado la producción a partir de glucosa . Las formas más avanzadas de abordar estos problemas se centran en las alternativas de electrificación al craqueo con vapor .
Almacenamiento y manipulación
El propeno es inflamable. El propeno generalmente se almacena como líquido a presión, aunque también es posible almacenarlo de manera segura como gas a temperatura ambiente en recipientes aprobados.
Ocurrencia en la naturaleza
El propeno se detecta en el medio interestelar mediante espectroscopía de microondas. El 30 de septiembre de 2013, la NASA también anunció que la nave espacial Cassini, parte de la misión Cassini-Huygens , había descubierto pequeñas cantidades de propeno natural en la atmósfera de Titán utilizando espectroscopía.
Ver también
- Desastre de Los Alfaques
- Abuso de inhalantes
- 2014 explosiones de gas de Kaohsiung
- 2020 explosión de Houston