2-butanol - 2-Butanol

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
Butan-2-ol |
|
| Otros nombres
sec -Butanol
sec -Alcohol butílico 2-Butanol Alcohol 2-butílico |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 773649 1718764 ( R ) |
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Tarjeta de información ECHA |
100.001.053 |
| Número CE | |
| 1686 396584 ( R ) |
|
| Malla | 2-butanol |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 1120 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 4 H 10 O | |
| Masa molar | 74,123 g · mol −1 |
| Densidad | 0,808 g cm −3 |
| Punto de fusion | -115 ° C; -175 ° F; 158 K |
| Punto de ebullición | 98 a 100 ° C; 208 a 212 ° F; 371 hasta 373 K |
| 290 g / L | |
| log P | 0,683 |
| Presión de vapor | 1,67 kPa (a 20 ° C) |
| Acidez (p K a ) | 17,6 |
| −5,7683 × 10 −5 cm 3 mol −1 | |
|
Índice de refracción ( n D )
|
1.3978 (a 20 ° C) |
| Termoquímica | |
|
Capacidad calorífica ( C )
|
197,1 J K −1 mol −1 |
|
Entropía molar estándar ( S |
213,1 J K −1 mol −1 |
| −343,3 a −342,1 kJ mol −1 | |
| −2,6611 a −2,6601 MJ mol −1 | |
| Peligros | |
| Ficha de datos de seguridad | inchem.org |
| Pictogramas GHS |
 
|
| Palabra de señal GHS | Advertencia |
| H226 , H319 , H335 , H336 | |
| P261 , P305 + 351 + 338 | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | 22 a 27 ° C (72 a 81 ° F; 295 a 300 K) |
| 405 ° C (761 ° F; 678 K) | |
| Límites explosivos | 1,7–9,8% |
| Dosis o concentración letal (LD, LC): | |
|
LC Lo ( menor publicado )
|
16.000 ppm (rata, 4 horas) 10.670 ppm (ratón, 3,75 horas) 16.000 ppm (ratón, 2,67 horas) |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
TWA 150 ppm (450 mg / m 3 ) |
|
REL (recomendado)
|
TWA 100 ppm (305 mg / m 3 ) ST 150 ppm (455 mg / m 3 ) |
|
IDLH (peligro inmediato)
|
2000 ppm |
| Compuestos relacionados | |
|
Butanoles relacionados
|
n -Butanol Isobutanol terc -Butanol |
|
Compuestos relacionados
|
Butanona |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
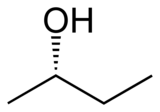
2-Butanol , o sec -butanol , es un compuesto orgánico con la fórmula C H 3 CH ( O H) CH 2 CH 3 . Este alcohol secundario es un líquido inflamable, incoloro, soluble en tres partes de agua y completamente miscible con disolventes orgánicos. Se produce a gran escala, principalmente como precursor del disolvente industrial metiletilcetona . El 2-butanol es quiral y, por tanto, puede obtenerse como cualquiera de los dos estereoisómeros designados como ( R ) - (-) - 2-butanol y ( S ) - (+) - 2-butanol. Normalmente se encuentra como una mezcla 1: 1 de los dos estereoisómeros, una mezcla racémica .
 |
|
 |

|
| ( R ) - (-) - 2-butanol | ( S ) - (+) - 2-butanol |
Fabricación y aplicaciones
El 2-butanol se fabrica industrialmente mediante la hidratación de 1-buteno o 2-buteno :
El ácido sulfúrico se utiliza como catalizador para esta conversión.
En el laboratorio se puede preparar mediante la reacción de Grignard haciendo reaccionar bromuro de etilmagnesio con acetaldehído en éter dietílico seco o tetrahidrofurano .
Aunque se usa algo de 2-butanol como solvente, se convierte principalmente en butanona (metiletilcetona, MEK), un solvente industrial importante que se encuentra en muchos agentes de limpieza domésticos y removedores de pintura. Aunque la mayoría de los removedores de pintura han dejado de usar MEK en sus productos debido a problemas de salud y nuevas leyes. Los ésteres volátiles de 2-butanol tienen aromas agradables y se utilizan en pequeñas cantidades como perfumes o en sabores artificiales.
Solubilidad
La solubilidad enumerada del 2-butanol a menudo es incorrecta, incluidas algunas de las referencias más conocidas, como el Merck Index , el CRC Handbook of Chemistry and Physics y el Lange's Handbook of Chemistry . Incluso el Programa Internacional de Seguridad Química enumera la solubilidad incorrecta. Este error generalizado se originó debido al Handbuch der Organischen Chemie ( Manual de química orgánica ) de Beilstein . Este trabajo cita una falsa solubilidad de 12,5 g / 100 g de agua. Muchas otras fuentes utilizaron esta solubilidad, que se ha convertido en un error generalizado en el mundo industrial. Los datos correctos (35,0 g / 100 ga 20 ° C, 29 g / 100 ga 25 ° C y 22 g / 100 ga 30 ° C) fueron publicados por primera vez en 1886 por Alexejew y luego otros datos similares fueron reportados por otros científicos como Dolgolenko y Dryer en 1907 y 1913, respectivamente.
Precauciones
Como otros butanoles, el 2-butanol tiene una baja toxicidad aguda. El LD 50 es 4400 mg / kg (rata, oral).
Se han reportado varias explosiones durante la destilación convencional de 2-butanol, aparentemente debido a la acumulación de peróxidos con un punto de ebullición más alto que el del alcohol puro (y por lo tanto se concentran en la olla destilada durante la destilación). Como los alcoholes, a diferencia de los éteres, no son ampliamente conocidos por ser capaces de formar impurezas de peróxido, es probable que se pase por alto el peligro. El 2-butanol se encuentra en las sustancias químicas que forman peróxido de clase B
Referencias
enlaces externos
- Tarjeta internacional de seguridad química 0112
- Guía de bolsillo de NIOSH sobre peligros químicos. "# 0077" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- IPCS Environmental Health Criteria 65: Butanoles: cuatro isómeros
- Guía de salud y seguridad 4 del IPCS : 2-butanol