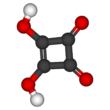
Ácido escuárico - Squaric acid
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
3,4-dihidroxiciclobut-3-eno-1,2-diona |
|||
| Otros nombres
Ácido cuadrático
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.018.875 |
||
|
PubChem CID
|
|||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 4 H 2 O 4 | |||
| Masa molar | 114,056 g · mol −1 | ||
| Apariencia | polvo cristalino blanco | ||
| Punto de fusion | > 300 ° C (572 ° F; 573 K) | ||
| Acidez (p K a ) | 1,5, 3,4 | ||
| Riesgos | |||
| Frases R (desactualizadas) | R36 / 37/38 R43 | ||
| Frases S (desactualizadas) | S26 S36 | ||
| punto de inflamabilidad | 190 ° C (374 ° F; 463 K) | ||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El ácido escuárico , también llamado ácido cuadrático porque sus cuatro átomos de carbono forman aproximadamente un cuadrado, es un ácido orgánico dibásico con la fórmula química C 4 O 2 (OH) 2 .
La base conjugada del ácido escuárico es el anión hidrogenosquarato C
4HO-
4; y la base conjugada del anión hidrogenocuadrado es el anión cuadrado divalente C
4O2−
4. Este es uno de los aniones oxocarbonados , que consta solo de carbono y oxígeno.
El ácido escuárico es un reactivo para la síntesis química , que se utiliza, por ejemplo, para fabricar colorantes de escuaraína fotosensibles e inhibidores de las proteínas tirosina fosfatasas .
Propiedades químicas
El ácido escuárico es un polvo cristalino blanco. El inicio de la descomposición térmica depende de las diferentes condiciones termodinámicas, como las velocidades de calentamiento.
La estructura del ácido escuárico no es un cuadrado perfecto, ya que las longitudes de los enlaces carbono-carbono no son del todo iguales. La alta acidez con p K a = 1,5 para el primer protón y p K a = 3,4 para el segundo es atribuible a la estabilización por resonancia del anión . Debido a que las cargas negativas se distribuyen por igual entre cada átomo de oxígeno, el dianión del ácido escuárico es completamente simétrico (a diferencia del propio ácido escuárico) con todas las longitudes de los enlaces C-C idénticas y todas las longitudes de los enlaces C-O idénticas.
Derivados
Muchas de las reacciones del ácido escuárico involucran a los grupos OH. La molécula se comporta de manera similar a un ácido dicarboxílico fuerte. Es un ácido más fuerte que los ácidos carboxílicos típicos.
- C 4 O 2 (OH) 2 → [C 4 O 3 (OH)] - + H + pK = 1,5
- [C 4 O 3 (OH)] - → [C 4 O 4 ] 2- + H + pK = 3,5
Los grupos OH son lábiles en ácido escuárico. Forma un dicloruro con cloruro de tionilo:
- C 4 O 2 (OH) 2 + 2 SOCl 2 → C 4 O 2 Cl 2 + 2 HCl + 2 SO 2
Los cloruros son buenos grupos salientes, que recuerdan a los cloruros de ácido . Son desplazados por diversos nucleófilos. De esta forma se puede preparar ditiioscuarato.
El bis (metiléter) se prepara mediante alquilación con ortoformiato de trimetilo .
Las escuramidas se preparan mediante el desplazamiento de grupos alcoxi o cloruro de C 4 O 2 X 2 (X = OR, Cl).
Uno o ambos de los grupos de oxígeno (= O) en el anión escuarato pueden reemplazarse por dicianometileno = C (CN) 2 . Los aniones resultantes, tales como 1,2-bis (dicianometileno) escuarato y 1,3-bis (dicianometileno) escuarato , conservan el carácter aromático del escuarato y se han denominado aniones pseudo-oxocarbonos .
La fotólisis del ácido escuárico en una matriz sólida de argón a 10 K (-263 ° C) proporciona acetilendiol .
Complejos de coordinación
El dianión cuadrado se comporta de manera similar al oxalato , formando complejos mono y polinucleares con iones de metales duros. Se puede preparar hidrato de escuadrato de cobalto (II) Co (C 4 O 4 ) (H 2 O) 2 (amarillo, cúbico) esterilizando en autoclave hidróxido de cobalto (II) y ácido escuárico en agua a 200 ° C. El agua está unida al átomo de cobalto , y la estructura cristalina consiste en una disposición cúbica de células huecas, cuyas paredes son seis aniones cuadrados (dejando un vacío de 7 Å de ancho) o varias moléculas de agua (dejando un vacío de 5 Å).
Se obtiene dihidróxido de escuarato de cobalto (II) Co 3 (OH) 2 (C 4 O 4 ) 2 · 3H 2 O (marrón) junto con el compuesto anterior. Tiene una estructura columnar que incluye canales llenos de moléculas de agua; estos se pueden quitar y reemplazar sin destruir la estructura cristalina. Las cadenas son ferromagnéticas ; se acoplan antiferromagnéticamente en forma hidratada, ferromagnéticamente en forma anhidra.
Se sintetizaron y caracterizaron complejos de ligandos mixtos diméricos y monoméricos escuarato de cobre (II). Se informan los espectros EPR infrarrojos, electrónicos y de banda Q, así como las susceptibilidades magnéticas.
El mismo método produce dihidróxido de escuarato de hierro (II) Fe 2 (OH) 2 (C 4 O 4 ) (marrón claro).
Síntesis
La síntesis original comenzó con la etanólisis del perfluorociclobuteno para dar 1,2-dietoxi-3,3,4,4-tetrafluoro-1-ciclobuteno. La hidrólisis da el ácido escuárico.
Aunque no es práctico, aniones cuadrados y relacionados como deltato C
3O2−
3y acetilendiolato C
2O2−
2se obtienen mediante acoplamiento reductor de monóxido de carbono utilizando complejos de organouranio .
Usos médicos
Médicamente, SADBE o éster de dibutilo de ácido escuárico o escuarato de dibutilo se deriva de un ácido escuárico. se utiliza para el tratamiento de verrugas . El éster dibutílico del ácido escuárico también se utiliza para tratar la alopecia areata o alopecia totalis ( caída del cabello autoinmune ) mediante inmunoterapia tópica que implica la producción de una erupción alérgica . El éster de dibutilo de ácido escuárico se encuentra actualmente en ensayos para su uso en el tratamiento del herpes labial (herpes labial).
Se utilizó dietilsquarato en la síntesis de Perzinfotel .
Los intentos de capitalizar el ácido escuárico en el campo de la química de las drogas también habían conducido al BMS-181885.
Ver también
-
Ciclobuteno , C
4H
6 -
Ácido deltico , C
3H
2O
3 -
Ácido crocónico , C
5H
2O
5 -
Ácido rodizónico , C
6H
2O
6 - Escuaramidas , las amidas de los ácidos escuáricos.