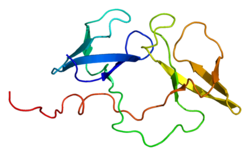
FMR1 - FMR1
FMR1 ( retraso mental del cromosoma X frágil 1 ) es un gen humano que codifica una proteína llamada proteína del retraso mental del cromosoma X frágil o FMRP. Esta proteína, que se encuentra más comúnmente en el cerebro, es esencial para el desarrollo cognitivo normaly la función reproductiva femenina. Las mutaciones de este gen pueden provocar síndrome de X frágil , discapacidad intelectual , insuficiencia ovárica prematura , autismo , enfermedad de Parkinson , retrasos en el desarrollo y otros déficits cognitivos. La premutación de FMR1 está asociada con un amplio espectro de fenotipos clínicosque afectan a más de dos millones de personas en todo el mundo.
Función
Plasticidad sinaptica
FMRP tiene una amplia gama de funciones en diferentes áreas de la neurona; sin embargo, estas funciones no se han caracterizado completamente. Se ha sugerido que la FMRP desempeña funciones en el transporte nucleocitoplasmático del ARNm , la localización del ARNm dendrítico y la síntesis de proteínas sinápticas . Los estudios del síndrome del X frágil han ayudado significativamente a comprender la funcionalidad de FMRP a través de los efectos observados de la pérdida de FMRP en las neuronas. Un modelo de ratón de retraso mental X frágil implicó la participación de FMRP en la plasticidad sináptica . La plasticidad sináptica requiere la producción de nuevas proteínas en respuesta a la activación de receptores sinápticos . Es la producción de proteínas en respuesta a la estimulación que se hipotetiza para permitir los cambios físicos permanentes y las conexiones sinápticas alteradas que están vinculadas con los procesos de aprendizaje y memoria.
La señalización del receptor de glutamato metabotrópico del grupo 1 (mGluR) se ha implicado en desempeñar un papel importante en la plasticidad sináptica dependiente de FMRP. La estimulación postsináptica de mGluR da como resultado la regulación positiva de la síntesis de proteínas a través de un segundo sistema mensajero . Un papel de mGluR en la plasticidad sináptica se evidencia aún más por la observación de la elongación de la columna dendrítica después de la estimulación de mGluR. Además, la activación de mGluR da como resultado la síntesis de FMRP cerca de las sinapsis . El FMRP producido se asocia con complejos polirribosomales después de la estimulación de mGluR, lo que propone la participación de la proteína de retraso mental X frágil en el proceso de traducción . Esto además aboga por un papel de FMRP en la síntesis de proteínas sinápticas y el crecimiento de conexiones sinápticas. La pérdida de FMRP da como resultado un fenotipo anormal de la columna dendrítica . Específicamente, la deleción del gen FMR1 en una muestra de ratones resultó en un aumento en el número de sinapsis de la columna.
Papel en la traducción
El mecanismo propuesto del efecto de FMRP sobre la plasticidad sináptica es a través de su papel como regulador negativo de la traducción. FMRP es una proteína de unión a ARN que se asocia con polirribosomas . Las capacidades de unión de ARN de FMRP dependen de sus dominios KH y cajas RGG. El dominio KH es un motivo conservado que caracteriza a muchas proteínas de unión a ARN. La mutagénesis de este dominio dio como resultado una unión de FMRP deteriorada al ARN.
Se ha demostrado que FMRP inhibe la traducción de ARNm. La mutación de la proteína FMRP dio como resultado la incapacidad de reprimir la traducción en contraposición a la contraparte de tipo salvaje que pudo hacerlo. Como se mencionó anteriormente, la estimulación de mGluR se asocia con un aumento de los niveles de proteína FMRP. Además, la estimulación de mGluR da como resultado un aumento de los niveles de ARNm diana de FMRP. Un estudio encontró que los niveles basales de proteínas codificadas por estos ARNm diana están significativamente elevados y mal regulados en ratones deficientes en FMRP.
La represión de la traducción de FMRP actúa inhibiendo el inicio de la traducción. FMRP se une directamente a CYFIP1 , que a su vez se une al factor de iniciación de la traducción eIF4E . El complejo FMRP-CYFIP1 prohíbe la iniciación dependiente de eIF4E, actuando así para reprimir la traducción. Cuando se aplica al fenotipo observado en el síndrome de X frágil, los niveles excesivos de proteína y la reducción del control de la traducción pueden explicarse por la pérdida de la represión de la traducción por FMRP en el síndrome de X frágil. FMRP actúa para controlar la traducción de un gran grupo de ARNm diana; sin embargo, se desconoce el alcance del control de traducción de los FMRP. Se ha demostrado que la proteína reprime la traducción de los ARNm diana en las sinapsis, incluidas las que codifican las proteínas citoesqueléticas Arc / Arg3.1 y MAP1B , y la CaM quinasa II . Además, FMRP se une a los ARNm de PSD-95 y GluR1 / 2. Es importante destacar que estos ARNm que se unen a FMRP desempeñan funciones importantes en la plasticidad neuronal.
Se ha demostrado que el control de la traducción de FMRP está regulado por la señalización de mGluR. La estimulación de mGluR puede resultar en el transporte de complejos de ARNm a las sinapsis para la síntesis de proteínas locales. Se ha demostrado que los gránulos de FMRP se localizan con ARNm de MAP1B y ARN ribosómico en las dendritas, lo que sugiere que este complejo en su conjunto puede necesitar ser transportado a las dendritas para la síntesis de proteínas locales. Además, se descubrió que los microtúbulos son un componente necesario para la translocación dependiente de mGluR de FMRP en dendritas. La FMRP puede desempeñar un papel adicional en la síntesis de proteínas locales al ayudar en la asociación de carga de ARNm y microtúbulos. Por tanto, FMRP puede regular la eficacia del transporte, así como la represión de la traducción durante el transporte. Finalmente, la síntesis, ubiquitinación y proteólisis de FMRP ocurren rápidamente en respuesta a la señalización de mGluR, lo que sugiere un papel extremadamente dinámico del regulador de traducción.
La expresion genica
El gen FMR1 se encuentra en el cromosoma X y contiene un trinucleótido CGG repetido. En la mayoría de las personas, el segmento CGG se repite aproximadamente de 5 a 44 veces. Un mayor número de repeticiones del segmento CGG se asocia con un deterioro de la función cognitiva y reproductiva. Si una persona tiene 45-54 repeticiones, esto se considera la "zona gris" o riesgo límite, 55-200 repeticiones se denomina premutación y más de 200 repeticiones se considera una mutación completa del gen FMR1 según el American College of Medical Genetics. y Genómica. La primera secuencia de ADN completa de la expansión repetida en alguien con la mutación completa fue generada por científicos en 2012 usando secuenciación SMRT . Este es un ejemplo de un trastorno de repetición de trinucleótidos . La expansión de la repetición de trinucleótidos es probablemente una consecuencia del deslizamiento de la hebra durante la reparación del ADN o la replicación del ADN .
FMR1 es una proteína de unión a cromatina que actúa en la respuesta al daño del ADN . FMR1 ocupa sitios en los cromosomas meióticos y regula la dinámica de la maquinaria de respuesta al daño del ADN durante la espermatogénesis .
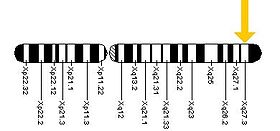
El gen FMR1 se puede encontrar en el brazo largo (q) del cromosoma X en la posición 27.3, desde el par de bases 146,699,054 al par de bases 146,738,156
Condiciones relacionadas
Síndrome X frágil
Casi todos los casos de síndrome de X frágil son causados por la expansión de la repetición del trinucleótido CGG en el gen FMR1 . En estos casos, la CGG se repite de forma anormal de 200 a más de 1000 veces. Como resultado, esta parte del gen FMR1 está metilada, lo que silencia el gen (se apaga y no produce ninguna proteína). Sin un FMR1 adecuado, se pueden desarrollar discapacidades graves del aprendizaje o discapacidades intelectuales, junto con anomalías físicas que se observan en el síndrome de X frágil.
Menos del 1% de todos los casos de síndrome de X frágil son causados por mutaciones que eliminan parte o todo el gen FMR1 , o cambian un par de bases, lo que lleva a un cambio en uno de los aminoácidos del gen. Estas mutaciones alteran la forma tridimensional de FMRP o impiden que la proteína se sintetice, lo que lleva a los signos y síntomas del síndrome de X frágil.
Una secuencia CGG en el gen FMR1 que se repite entre 55 y 200 veces se describe como una premutación. Aunque la mayoría de las personas con la premutación son intelectualmente normales, algunas de estas personas tienen versiones leves de las características físicas que se observan en el síndrome de X frágil (como orejas prominentes) y pueden experimentar problemas de salud mental como ansiedad o depresión.
Síndrome de ataxia / temblor asociado al cromosoma X frágil
Las premutaciones están asociadas con un mayor riesgo de síndrome de ataxia / temblor asociado al cromosoma X frágil (FXTAS). FXTAS se caracteriza por ataxia (pérdida de coordinación), temblor , pérdida de memoria , pérdida de sensibilidad en las extremidades inferiores ( neuropatía periférica ) y cambios mentales y de comportamiento. El trastorno generalmente se desarrolla en una etapa avanzada de la vida.
Envejecimiento ovárico prematuro
El gen FMR1 juega un papel muy importante en la función ovárica, independientemente de los efectos cognitivos / neurológicos. Las expansiones menores de las repeticiones CGG que no causan el síndrome de X frágil se asocian con un mayor riesgo de envejecimiento ovárico prematuro , también llamada insuficiencia ovárica primaria oculta, una afección en la que las mujeres agotan prematuramente su función ovárica.
Síndrome de ovario poliquístico
Se ha encontrado que un subgenotipo muy específico de FMR1 está asociado con el síndrome de ovario poliquístico (SOP). La expresión genética, denominada heterocigoto-normal / baja, puede causar una actividad folicular excesiva similar al síndrome de ovario poliquístico y una función ovárica hiperactiva cuando las mujeres son más jóvenes.
Interacciones
Se ha demostrado que FMR1 interactúa con:
Referencias
Otras lecturas
- Bassell GJ, Warren ST (octubre de 2008). "Síndrome de X frágil: la pérdida de la regulación local del ARNm altera el desarrollo y la función sináptica" . Neurona . 60 (2): 201-14. doi : 10.1016 / j.neuron.2008.10.004 . PMC 3691995 . PMID 18957214 .
- Hagerman PJ, Hagerman RJ (mayo de 2004). "La premutación del X frágil: una perspectiva de maduración" . Revista Estadounidense de Genética Humana . 74 (5): 805–16. doi : 10.1086 / 386296 . PMC 1181976 . PMID 15052536 .
- Hagerman RJ, Leavitt BR, Farzin F, Jacquemont S, Greco CM, Brunberg JA, Tassone F, Hessl D, Harris SW, Zhang L, Jardini T, Gane LW, Ferranti J, Ruiz L, Leehey MA, Grigsby J, Hagerman PJ (Mayo de 2004). "Síndrome de ataxia / temblor asociado al cromosoma X frágil (FXTAS) en mujeres con la premutación FMR1" . Revista Estadounidense de Genética Humana . 74 (5): 1051–6. doi : 10.1086 / 420700 . PMC 1181968 . PMID 15065016 .
- Jacquemont S, Hagerman RJ, Leehey MA, Hall DA, Levine RA, Brunberg JA, Zhang L, Jardini T, Gane LW, Harris SW, Herman K, Grigsby J, Greco CM, Berry-Kravis E, Tassone F, Hagerman PJ ( Enero de 2004). "Penetrancia del síndrome de ataxia / temblor asociado a X frágil en una población portadora de premutación" . JAMA . 291 (4): 460–9. doi : 10.1001 / jama.291.4.460 . PMID 14747503 .
- Jin P, Alisch RS, Warren ST (noviembre de 2004). "ARN y microARN en retraso mental X frágil". Biología celular de la naturaleza . 6 (11): 1048–53. doi : 10.1038 / ncb1104-1048 . PMID 15516998 . S2CID 7315938 .
- Jin P, Warren ST (marzo de 2003). "Nuevos conocimientos sobre el síndrome de X frágil: de moléculas a neurocomportamientos". Tendencias en Ciencias Bioquímicas . 28 (3): 152–8. CiteSeerX 10.1.1.532.4162 . doi : 10.1016 / S0968-0004 (03) 00033-1 . PMID 12633995 .
- O'Donnell WT, Warren ST (2002). "Una década de estudios moleculares del síndrome de X frágil". Revisión anual de neurociencia . 25 : 315–38. doi : 10.1146 / annurev.neuro.25.112701.142909 . PMID 12052912 .
- Oostra BA, Chiurazzi P (diciembre de 2001). "El gen X frágil y su función". Genética clínica . 60 (6): 399–408. doi : 10.1034 / j.1399-0004.2001.600601.x . PMID 11846731 . S2CID 40128119 .
- Oostra BA, Willemsen R (octubre de 2003). "Un equilibrio frágil: niveles de expresión de FMR1" . Genética molecular humana . 12 Especificación nº 2 (90002): R249–57. doi : 10.1093 / hmg / ddg298 . PMID 12952862 .
- Nicola NA, Metcalf D (octubre de 1991). "Promiscuidad de subunidades entre los receptores del factor de crecimiento hematopoyético". Celular . 67 (1): 1–4. doi : 10.1016 / 0092-8674 (91) 90564-F . PMID 1913811 . S2CID 12696714 .
- Sielska D, Milewski M, Bal J (2003). "[Patogenia molecular del síndrome de X frágil]". Medycyna Wieku Rozwojowego . 6 (4): 295-308. PMID 12810982 .
- Bagni C, Greenough WT (mayo de 2005). "Del tráfico de mRNP a la dismorfogénesis de la columna: las raíces del síndrome de X frágil" . Reseñas de la naturaleza. Neurociencia . 6 (5): 376–87. doi : 10.1038 / nrn1667 . PMID 15861180 . S2CID 17374547 .
- Huber KM (abril de 2006). "La frágil conexión X-cerebelo". Tendencias en neurociencias . 29 (4): 183–5. doi : 10.1016 / j.tins.2006.02.001 . PMID 16500716 . S2CID 8674692 .
- Loesch DZ, Bui QM, Dissanayake C, Clifford S, Gould E, Bulhak-Paterson D, Tassone F, Taylor AK, Hessl D, Hagerman R, Huggins RM (2007). "Predictores moleculares y cognitivos del continuo de comportamientos autistas en X frágil" . Revisiones de neurociencia y bioconducta . 31 (3): 315-26. doi : 10.1016 / j.neubiorev.2006.09.007 . PMC 2145511 . PMID 17097142 .