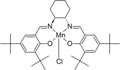C 2 -Ligandos simétricos - C2-Symmetric ligands
En la catálisis homogénea , los ligandos simétricos C 2 se refieren a ligandos que carecen de simetría especular pero tienen simetría C 2 (simetría rotacional doble). Dichos ligandos suelen ser bidentados y son valiosos en catálisis . La simetría C 2 de los ligandos limita el número de posibles vías de reacción y, por tanto, aumenta la enantioselectividad , en relación con los análogos asimétricos. Los ligandos asimétricos C 2 son un subconjunto de ligandos quirales. Los ligandos quirales, incluidos los ligandos asimétricos C 2 , se combinan con metales u otros grupos para formar catalizadores quirales . Estos catalizadores participan en la síntesis química enantioselectiva , en la que la quiralidad en el catalizador produce quiralidad en el producto de reacción.
Ejemplos de
Uno de los primeros C 2 ligando -symmetric, difosfina ligando catalítica DIPAMP , fue desarrollado en 1968 por William S. Knowles y compañeros de trabajo de la empresa Monsanto , que compartió el 2001 Premio Nobel de Química . Este ligando se utilizó en la producción industrial de L- DOPA .
Algunas clases de ligandos asimétricos C 2 se denominan ligandos privilegiados , que son ligandos que son ampliamente aplicables a múltiples procesos catalíticos, no solo a un solo tipo de reacción.
- Ligandos y complejos
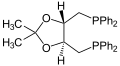
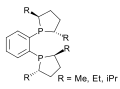
Los ligandos DuPhos son una clase de ligandos asimétricos C 2 para hidrogenación asimétrica .
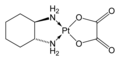
El oxaliplatino , que contiene el C 2 -symmetric ( R , R ) diaminociclohexano ligando, es un importante fármaco anticanceroso .
El catalizador de epoxidación de Jacobsen es un complejo de un ligando de tipo salen C 2 asimétrico .
Los ligandos bis (oxazolina) bidentados y tridentados se utilizan en la síntesis orgánica.
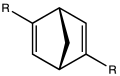
Ambos enantiómeros de BINAP
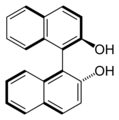
BINOL , otro ligando a base de binaftaleno
DIPAMP , una difosfina de importancia histórica
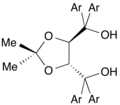
AD-mix α, derivado de dihidroquinina utilizado en dihidroxilación asimétrica Sharpless
Conceptos mecanicistas
Si bien la presencia de cualquier elemento de simetría dentro de un ligando destinado a la inducción asimétrica puede parecer contradictorio, la inducción asimétrica solo requiere que el ligando sea quiral (es decir, que no tenga un eje de rotación inadecuado ). No se requiere asimetría (es decir, ausencia de elementos de simetría ). La simetría C 2 mejora la enantioselectividad del complejo al reducir el número de geometrías únicas en los estados de transición . Los factores estéricos y cinéticos suelen favorecer la formación de un solo producto.

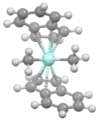
Cerca quiral
Los ligandos quirales funcionan por inducción asimétrica en algún lugar a lo largo de la coordenada de reacción . La imagen de la derecha ilustra cómo un ligando quiral puede inducir una reacción enantioselectiva. El ligando (en verde) tiene simetría C 2 con sus átomos de nitrógeno, oxígeno o fósforo abrazando un átomo metálico central (en rojo). En este ligando en particular, el lado derecho sobresale y el lado izquierdo apunta hacia afuera. El sustrato en esta reducción es acetofenona y el reactivo (en azul) un ion hidruro . En ausencia del metal y del ligando, el enfoque de la cara Re del ion hidruro da el enantiómero ( S ) y el enfoque de la cara de Si el enantiómero ( R ) en cantidades iguales (una mezcla racémica como la esperada). La presencia de ligandos y metales cambia todo eso. El grupo carbonilo se coordinará con el metal y debido al volumen estérico del grupo fenilo solo podrá hacerlo con su cara de Si expuesta al ion hidruro con, en la situación ideal, formación exclusiva del enantiómero ( R ). La re cara simplemente golpeará la cerca quiral . Tenga en cuenta que cuando el ligando se reemplaza por su imagen especular, se formará el otro enantiómero y que una mezcla racémica de ligando volverá a producir un producto racémico. También tenga en cuenta que si el volumen estérico de ambos sustituyentes carbonilo es muy similar, la estrategia fallará.
Otros complejos C 2 asimétricos
Se conocen muchos complejos C 2 asimétricos. Algunos surgen no de ligandos asimétricos C 2 , sino de la orientación o disposición de ligandos de alta simetría dentro de la esfera de coordinación del metal. En particular, el EDTA y la trietilentetraamina forman complejos que son simétricos en C 2 en virtud de la forma en que los ligandos se envuelven alrededor de los centros metálicos. Son posibles dos isómeros para ( indenil ) 2 MX 2 , C s - y C 2 - simétrico. Los complejos C2 - asimétricos son ópticamente estables.
- Otro C <sub
C 2 -symmetric de metal-EDTA quelato como se encuentra en complejos de Co (III).
Ligandos asimétricos
Los ligandos que contienen centros de quiralidad atómica como el carbono asimétrico , que normalmente no tienen simetría C 2 , siguen siendo importantes en la catálisis. Los ejemplos incluyen alcaloides de cinchona y ciertas fosforamiditas . También se han investigado las P-monofosfinas quirales .
Ver también
Otras lecturas
- Desimoni, G .; Faita, G .; Jorgensen, KA (2006). " Ligandos de bis (oxazolina) quirales asimétricos C 2 en catálisis asimétrica". Chem. Rev . 106 (9): 3561–3651. doi : 10.1021 / cr0505324 . PMID 16967916 .
- Liu, X .; Lin, L .; Feng, X. (2011). "N, N'-dióxidos quirales: nuevos ligandos y organocatalizadores para reacciones asimétricas catalíticas". Acc. Chem. Res . 44 páginas = 574-587 (8): 574–87. doi : 10.1021 / ar200015s . PMID 21702458 .
- Evans, DA; Kozlowski, MC; Murry, JA; Burgey, CS; Campos, KR; Connell, BT; Grapas, RJ (1999). " Complejos de cobre (II) simétricos C 2 como ácidos quirales de Lewis. Alcance y mecanismo de las adiciones catalíticas enantioselectivas de aldol de enolsilanos a (benciloxi) acetaldehído". Mermelada. Chem. Soc . 121, 669–685 (4): 669–685. doi : 10.1021 / JA9829822 .
- Gao, J.-X .; Ikariya, T .; Noyori, R. (1996). "Un complejo de rutenio (II) con un ligando tetradentado de diamina / difosfina simétrica C 2 para la hidrogenación de transferencia asimétrica de cetonas aromáticas". Organometálicos . 15 : 1087–1089. doi : 10.1021 / OM950833B .
- Pye, PJ; Rossen, K .; Escariador, RA; Tsou, NN; Volante, RP; Reider, PJ (1997). "Nuevo ligando de bisfosfina quiral planar para catálisis asimétrica: hidrogenaciones altamente enantioselectivas en condiciones suaves". Mermelada. Chem. Soc . 119 (26): 6207–6208. doi : 10.1021 / JA970654G .