Pentafluoruro de antimonio - Antimony pentafluoride
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC
fluoruro de antimonio (V)
|
|||
| Otros nombres
pentafluoruro de antimonio
pentafluoridoantimonio |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.029.110 |
||
| Número CE | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| un numero | 1732 | ||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| SbF 5 | |||
| Masa molar | 216,74 g / mol | ||
| Apariencia | higroscópico líquido aceitoso incoloro |
||
| Olor | acre | ||
| Densidad | 2,99 g / cm 3 | ||
| Punto de fusion | 8,3 ° C (46,9 ° F; 281,4 K) | ||
| Punto de ebullición | 149,5 ° C (301,1 ° F; 422,6 K) | ||
| Reacciona | |||
| Solubilidad | soluble en KF , SO 2 líquido | ||
| Peligros | |||
| Principales peligros | Libera ácido fluorhídrico al entrar en contacto con agua o tejidos biológicos | ||
| Ficha de datos de seguridad | ICSC 0220 | ||
| Pictogramas GHS |
  
|
||
| Palabra de señal GHS | Peligro | ||
| H302 , H314 , H332 , H411 , H412 | |||
| P260 , P261 , P264 , P270 , P271 , P273 , P280 , P301 + 312 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 312 , P304 + 340 , P305 + 351 + 338 , P310 , P312 , P321 , P330 , P363 , P391 , P405 , P501 | |||
| NFPA 704 (diamante de fuego) | |||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
|
PEL (permitido)
|
TWA 0,5 mg / m 3 (como Sb) | ||
|
REL (recomendado)
|
TWA 0,5 mg / m 3 (como Sb) | ||
| Compuestos relacionados | |||
|
Otros aniones
|
Pentacloruro de antimonio | ||
|
Otros cationes
|
Pentafluoruro de fósforo Pentafluoruro de arsénico Pentafluoruro de bismuto |
||
|
Compuestos relacionados
|
Trifluoruro de antimonio | ||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
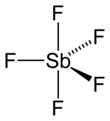
El pentafluoruro de antimonio es el compuesto inorgánico de fórmula Sb F 5 . Este líquido viscoso e incoloro es un valioso ácido de Lewis y un componente del ácido fluoroantimónico superácido , formado al mezclar HF líquido con SbF 5 líquido en una proporción de 2: 1. Destaca por su acidez de Lewis y su capacidad para reaccionar con casi todos los compuestos conocidos.
Preparación
El pentafluoruro de antimonio se prepara mediante la reacción del pentacloruro de antimonio con fluoruro de hidrógeno anhidro :
- SbCl 5 + 5 HF → SbF 5 + 5 HCl
También se puede preparar a partir de trifluoruro de antimonio y flúor.
Estructura y reacciones químicas
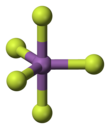
En la fase gaseosa, SbF 5 adopta una estructura bipiramidal trigonal de simetría de grupo de puntos D 3h (ver imagen). El material adopta una estructura más complicada en los estados líquido y sólido. El líquido contiene polímeros en los que cada Sb es octaédrico, la estructura se describe con la fórmula [SbF 4 (μ-F) 2 ] n ((μ-F) denota el hecho de que los centros de fluoruro forman un puente entre dos centros Sb). El material cristalino es un tetrámero, lo que significa que tiene la fórmula [SbF 4 (μ-F)] 4 . Los enlaces Sb-F son 2,02 Å dentro del anillo Sb 4 F 4 de ocho miembros ; los ligandos de fluoruro restantes que irradian desde los cuatro centros Sb son más cortos a 1,82 Å. Las especies relacionadas PF 5 y AsF 5 son monoméricas en los estados sólido y líquido, probablemente debido a los tamaños más pequeños del átomo central, lo que limita su número de coordinación. BiF 5 es un polímero.
De la misma manera que SbF 5 mejora la acidez Brønsted del HF, aumenta el poder oxidante del F 2 . Este efecto está ilustrado por la oxidación del oxígeno :
- 2 SbF 5 + F 2 + 2 O 2 → 2 [O 2 ] + [SbF 6 ] -
El pentafluoruro de antimonio también se ha utilizado en la primera reacción química descubierta que produce gas flúor a partir de compuestos de fluoruro:
- 4 SbF
5 + 2 K
2 MnF
6 → 4 KSbF
6 + 2 MnF
3 + F
2
La fuerza impulsora de esta reacción es la alta afinidad de SbF 5 por F -
, que es la misma propiedad que recomienda el uso de SbF 5 para generar superácidos.
Hexafluoroantimoniato
El SbF 5 es un ácido de Lewis fuerte, excepcionalmente hacia las fuentes de F - para dar el anión muy estable [SbF 6 ] - , llamado hexafluoroantimoniato. [SbF 6 ] - es un anión de coordinación débil similar a PF 6 - . Aunque es solo débilmente básico, [SbF 6 ] - reacciona con SbF 5 adicional para dar un aducto centrosimétrico :
- SbF 5 + [SbF 6 ] - → [Sb 2 F 11 ] -
La seguridad
El SbF 5 reacciona violentamente con muchos compuestos, a menudo liberando peligroso fluoruro de hidrógeno . Es corrosivo para la piel y los ojos.