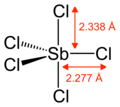
Pentacloruro de antimonio - Antimony pentachloride
|
|
|||

|
|||
| Nombres | |||
|---|---|---|---|
|
Nombres IUPAC
Pentacloruro de
antimonio Cloruro de antimonio (V) |
|||
| Otros nombres
Cloruro
antimónico Percloruro de antimonio |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.028.729 |
||
| Número CE | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| Cl 5 Sb | |||
| Masa molar | 299,01 g · mol −1 | ||
| Apariencia | líquido incoloro o amarillo rojizo (humeante), aceitoso | ||
| Olor | picante, ofensivo | ||
| Densidad | 2,336 g / cm 3 (20 ° C) 2,36 g / cm 3 (25 ° C) |
||
| Punto de fusion | 2,8 ° C (37,0 ° F; 275,9 K) | ||
| Punto de ebullición | 140 ° C (284 ° F; 413 K) se descompone de 106 ° C 79 ° C (174 ° F; 352 K) a 22 mmHg 92 ° C (198 ° F; 365 K) a 30 mmHg |
||
| reacciona | |||
| Solubilidad | soluble en alcohol , HCl , ácido tartárico , CHCl 3 , CS 2 , CCl 4 | ||
| Solubilidad en oxicloruro de selenio (IV) | 62,97 g / 100 g (25 ° C) | ||
| Presión de vapor | 0,16 kPa (25 ° C) 4 kPa (40 ° C) 7,7 kPa (100 ° C) |
||
| -120,0 · 10 −6 cm 3 / mol | |||
|
Índice de refracción ( n D )
|
1.59255 | ||
| Viscosidad | 2,034 cP (29,4 ° C) 1,91 cP (35 ° C) |
||
| Estructura | |||
| Triangular bipiramidal | |||
| 0 D | |||
| Termoquímica | |||
|
Capacidad calorífica ( C )
|
120,9 J / mol · K (gas) | ||
|
Entropía molar estándar ( S |
295 J / mol · K | ||
| -437,2 kJ / mol | |||
|
Energía libre de Gibbs (Δ f G ˚)
|
-345,35 kJ / mol | ||
| Peligros | |||
| Pictogramas GHS |
 
|
||
| Palabra de señal GHS | Peligro | ||
| H314 , H411 | |||
| P273 , P280 , P305 + 351 + 338 , P310 | |||
| Peligro de inhalación | Tóxico | ||
| NFPA 704 (diamante de fuego) | |||
| punto de inflamabilidad | 77 ° C (171 ° F; 350 K) | ||
| Dosis o concentración letal (LD, LC): | |||
|
LD 50 ( dosis media )
|
1115 mg / kg, (rata, oral) | ||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
|
PEL (permitido)
|
TWA 0,5 mg / m 3 (como Sb) | ||
|
REL (recomendado)
|
TWA 0,5 mg / m 3 (como Sb) | ||
| Compuestos relacionados | |||
|
Otros aniones
|
Pentafluoruro de antimonio | ||
|
Otros cationes
|
Pentacloruro de fósforo | ||
|
Compuestos relacionados
|
Tricloruro de antimonio | ||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El pentacloruro de antimonio es un compuesto químico con la fórmula SbCl 5 . Es un aceite incoloro, pero las muestras típicas son amarillentas debido a las impurezas. Debido a su tendencia a hidrolizarse a ácido clorhídrico , el SbCl 5 es una sustancia altamente corrosiva y debe almacenarse en recipientes de vidrio o PTFE .
Preparación y estructura
El pentacloruro de antimonio se prepara pasando cloro gaseoso en tricloruro de antimonio fundido :
- SbCl 3 + Cl 2 → SbCl 5
El SbCl 5 gaseoso tiene una estructura bipiramidal trigonal.
Reacciones
El pentacloruro de antimonio se hidroliza para dar ácido clorhídrico y oxicloruros de antimonio . Esta reacción se suprime en presencia de un gran exceso de cloruro, debido a la formación del ion complejo hexacloroantimoniato :
- SbCl 5 + Cl - → [SbCl 6 ] -
Se conocen los mono y tetrahidratos, SbCl 5 · H 2 O y SbCl 5 · 4H 2 O.
Este compuesto forma aductos con muchas bases de Lewis. El SbCl 5 es un ácido de Lewis blando y sus parámetros del modelo ECW son E A = 3.64 y C A = 10.42. Se utiliza como ácido de Lewis estándar en la escala Gutmann de basicidad de Lewis .
También es un agente oxidante fuerte . Por ejemplo, los éteres aromáticos se oxidan a sus cationes radicales de acuerdo con la siguiente estequiometría:
- 3 SbCl 5 + 2 ArH → 2 (ArH +) (SbCl 6 - ) + SbCl 3
Aplicaciones
El pentacloruro de antimonio se utiliza como catalizador de polimerización y para la cloración de compuestos orgánicos.
Precauciones
El pentacloruro de antimonio es una sustancia altamente corrosiva que debe almacenarse lejos del calor y la humedad. Es un agente clorante y, en presencia de humedad, libera gas cloruro de hidrógeno. Debido a esto, puede grabar incluso herramientas de acero inoxidable (como agujas), si se manipula en una atmósfera húmeda. No debe manipularse con plásticos no fluorados (como jeringas de plástico, tabiques de plástico o agujas con accesorios de plástico), ya que derrite y carboniza los materiales plásticos.