Cloruro de indio (III) - Indium(III) chloride
|
|
| Nombres | |
|---|---|
| Otros nombres
Cloruro de
indio Tricloruro de indio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.030.027 |
| Número CE | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 3260 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| InCl 3 | |
| Masa molar | 221,18 g / mol |
| Apariencia | copos blancos |
| Densidad | 3,46 g / cm 3 |
| Punto de fusion | 586 ° C (1.087 ° F; 859 K) |
| Punto de ebullición | 800 ° C (1.470 ° F; 1.070 K) |
| 195 g / 100 mL, exotérmico | |
| Solubilidad en otros disolventes | THF , etanol |
| Estructura | |
| Monoclínico , MS16 | |
| C12 / m1, No. 12 | |
| Riesgos | |
| Principales peligros | Corrosivo |
| Ficha de datos de seguridad | SDS externo |
| Pictogramas GHS |
 
|
| Palabra de señal GHS | Peligro |
| H302 , H314 | |
| P260 , P303 + 361 + 353 , P305 + 351 + 338 , P301 + 330 + 331 , P405 , P501 | |
| NFPA 704 (diamante de fuego) | |
| Compuestos relacionados | |
|
Otros aniones
|
Fluoruro de indio (III) Bromuro de indio (III) Yoduro de indio (III) |
|
Otros cationes
|
Cloruro de aluminio Tricloruro de galio Cloruro de talio (III) |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El cloruro de indio (III) es el compuesto químico con la fórmula In Cl 3 . Esta sal es un sólido blanco en escamas con aplicaciones en síntesis orgánica como ácido de Lewis . También es el derivado soluble del indio más disponible.
Síntesis y estructura
Al ser un metal relativamente electropositivo, el indio reacciona rápidamente con el cloro para dar el tricloruro. El tricloruro de indio es muy soluble y delicuescente. Se ha informado de una síntesis utilizando una celda electroquímica en una solución mixta de metanol y benceno .
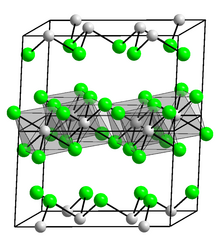
Al igual que el AlCl 3 y el TlCl 3 , el InCl 3 cristaliza como una estructura en capas que consta de una disposición de cloruro compacta que contiene capas de centros de In (III) coordinados octaédricamente , una estructura similar a la que se observa en el YCl 3 . En contraste, GaCl 3 cristaliza como dímeros que contienen Ga 2 Cl 6 . El InCl 3 fundido conduce la electricidad, mientras que el AlCl 3 no lo hace ya que se convierte en el dímero molecular, Al 2 Cl 6 .
Reacciones
InCl 3 es un ácido de Lewis y forma complejos con ligandos donantes , L, InCl 3 L, InCl 3 L 2 , InCl 3 L 3 . Por ejemplo, con el ion cloruro forma InCl 4 - tetraédrico , InCl 5 2− bipiramidal trigonal e InCl 6 3− octaédrico .
En solución de éter dietílico , InCl 3 reacciona con hidruro de litio , LiH, para formar . Este compuesto inestable se descompone por debajo de 0 ° C y se hace reaccionar in situ en síntesis orgánica como agente reductor y para preparar complejos de amina terciaria y fosfina de InH 3 .
El trimetilindio , InMe 3 , se puede producir haciendo reaccionar InCl 3 en una solución de éter dietílico con el reactivo de Grignard o con metil - litio , LiMe. El trietilindio se puede preparar de manera similar pero con el reactivo de Grignard EtMgBr.
El InCl 3 reacciona con el metal indio a alta temperatura para formar los cloruros de indio de menor valencia en 5 Cl 9 , In 2 Cl 3 e InCl.
Catalizador en química
El cloruro de indio es un catalizador ácido de Lewis en reacciones orgánicas como las acilaciones de Friedel-Crafts y las reacciones de Diels-Alder . Como ejemplo de lo último, la reacción se desarrolla a temperatura ambiente , con una carga de catalizador de 1% en moles en una mezcla de acetonitrilo- agua disolvente. El primer paso es una condensación de Knoevenagel entre el ácido barbitúrico y el aldehído; el segundo paso es una reacción de Diels-Alder con demanda de electrones inversa , que es una reacción de múltiples componentes de ácido N, N'-dimetilbarbitúrico , benzaldehído y etilviniléter . Con el catalizador, el rendimiento químico informado es del 90% y el porcentaje de isómero trans es del 70%. Sin el catalizador añadido, el rendimiento cae al 65% con un 50% de producto trans.







