Toxina diftérica - Diphtheria toxin
| precursor de la toxina de la difteria | |||||||
|---|---|---|---|---|---|---|---|
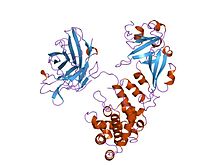 Representación de dibujos animados de la proteína de la toxina diftérica
| |||||||
| Identificadores | |||||||
| Organismo | |||||||
| Símbolo | tox | ||||||
| Entrez | 2650491 | ||||||
| RefSeq (Prot) | NP_938615 | ||||||
| UniProt | P00587 | ||||||
| Otros datos | |||||||
| Número CE | 2.4.2.36 | ||||||
| Cromosoma | genoma: 0,19 - 0,19 Mb | ||||||
| |||||||
| Toxina diftérica, dominio C | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Difteria_C | ||||||||
| Pfam | PF02763 | ||||||||
| Clan pfam | CL0084 | ||||||||
| InterPro | IPR022406 | ||||||||
| SCOP2 | 1ddt / SCOPe / SUPFAM | ||||||||
| TCDB | 1.C.7 | ||||||||
| |||||||||
| Toxina diftérica, dominio T | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Difteria_T | ||||||||
| Pfam | PF02764 | ||||||||
| InterPro | IPR022405 | ||||||||
| SCOP2 | 1ddt / SCOPe / SUPFAM | ||||||||
| TCDB | 1.C.7 | ||||||||
| |||||||||
| Toxina diftérica, dominio R | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Difteria_R | ||||||||
| Pfam | PF01324 | ||||||||
| InterPro | IPR022404 | ||||||||
| SCOP2 | 1ddt / SCOPe / SUPFAM | ||||||||
| TCDB | 1.C.7 | ||||||||
| |||||||||
La toxina diftérica es una exotoxina secretada por Corynebacterium , la bacteria patógena que causa la difteria . El gen de la toxina está codificado por un profago llamado corinefago β . La toxina causa la enfermedad en humanos al ingresar al citoplasma celular e inhibir la síntesis de proteínas .
Estructura
La toxina diftérica es una cadena polipeptídica única de 535 aminoácidos que consta de dos subunidades unidas por puentes disulfuro , conocida como toxina AB . La unión a la superficie celular de la subunidad B (la menos estable de las dos subunidades) permite que la subunidad A (la parte más estable de la proteína) penetre en la célula huésped .
La estructura cristalina del homodímero de la toxina diftérica se ha determinado con una resolución de 2,5 Ångstrom . La estructura revela una molécula en forma de Y que consta de tres dominios . El fragmento A contiene el dominio C catalítico y el fragmento B consta de los dominios T y R:
- El dominio catalítico amino-terminal , conocido como dominio C, tiene un pliegue beta + alfa inusual . El dominio C bloquea la síntesis de proteínas mediante la transferencia de ADP-ribosa de NAD a un residuo de diftamida del factor de elongación eucariota 2 (eEF-2).
- Un dominio de translocación central, conocido como dominio T o dominio TM, tiene un pliegue similar a la globina de múltiples hélices con dos hélices adicionales en el extremo amino terminal, pero sin contraparte de la primera hélice de globina . Se cree que este dominio se desarrolla en la membrana . Un cambio conformacional inducido por el pH en el dominio T desencadena la inserción en la membrana endosomal y facilita la transferencia del dominio C al citoplasma .
- Un dominio de unión al receptor carboxi-terminal , conocido como dominio R, tiene un pliegue en sándwich beta que consta de nueve hebras en dos hojas con topología de clave griega; es una subclase de pliegue similar a inmunoglobulina . El dominio R se une a un receptor de la superficie celular , lo que permite que la toxina entre en la célula por endocitosis mediada por el receptor .
Mecanismo
- Procesando
- La región líder se escinde durante la secreción.
- El corte proteolítico separa las subunidades A y B, que permanecen unidas por enlaces disulfuro hasta que alcanzan el citosol.
- La toxina se une al precursor del factor de crecimiento epidérmico de unión a heparina (HB-EGF).
- El complejo sufre endocitosis por la célula huésped.
- La acidificación dentro del endosoma induce la translocación de la subunidad A al citosol.
- Los enlaces disulfuro se rompen.
- La subunidad B permanece en el endosoma como un poro.
- Los ADP-ribosilatos de la subunidad A albergan eEF-2. Se requiere eEF-2 para la síntesis de proteínas; cuando se inactiva, el huésped no puede producir proteínas y, por lo tanto, muere.
La toxina diftérica tiene el mismo mecanismo de acción que la enzima NAD (+) - diftamida ADP-ribosiltransferasa ( EC 2.4.2.36 ). Cataliza la transferencia de NAD + a un residuo de diftamida en eEF-2, inactivando esta proteína. Lo hace mediante ADP-ribosilación del inusual aminoácido diftamida . De esta forma, actúa como inhibidor de la traducción del ARN . La reacción catalizada es la siguiente:
- NAD + + péptido diftamida nicotinamida + péptido N - (ADP-D-ribosil) diftamida.
La exotoxina A de Pseudomonas aeruginosa utiliza un mecanismo de acción similar.
Dosis y efectos letales
La toxina diftérica es extraordinariamente potente. La dosis letal para los seres humanos es de aproximadamente 0,1 μg de toxina por kg de peso corporal. La muerte ocurre por necrosis del corazón y el hígado . La toxina diftérica también se ha asociado con el desarrollo de miocarditis. La miocarditis secundaria a la toxina diftérica se considera uno de los mayores riesgos para los niños no vacunados.
Historia
La toxina diftérica fue descubierta en 1888 por Émile Roux y Alexandre Yersin . En 1890, Emil Adolf von Behring desarrolló una anti-toxina a base de sangre de caballos inmunizados con bacterias atenuadas. En 1951, Freeman descubrió que el gen de la toxina no estaba codificado en el cromosoma bacteriano, sino por un fago lisogénico ( corinefago β ) que infectaba todas las cepas toxigénicas.
Uso clínico
El fármaco denileucina diftitox utiliza la toxina diftérica como agente antineoplásico .
Resimmune es una inmunotoxina que se encuentra en ensayos clínicos en pacientes con linfoma cutáneo de células T. Utiliza toxina diftérica (truncada por el dominio de unión celular) acoplada a un anticuerpo contra CD3ε (UCHT1).
Investigar
Al igual que otras toxinas AB, la toxina diftérica es experta en el transporte de proteínas exógenas a través de las membranas celulares de los mamíferos, que suelen ser impermeables a las proteínas grandes. Esta capacidad única se puede reutilizar para administrar proteínas terapéuticas, en lugar del dominio catalítico de la toxina.
Esta toxina también se ha utilizado en la investigación neurocientífica y del cáncer para extirpar poblaciones específicas de células que expresan el receptor de la toxina diftérica ( factor de crecimiento similar a EGF de unión a heparina ). La administración de la toxina en el organismo que no expresa naturalmente este receptor (por ejemplo, ratones) dará como resultado la ablación selectiva de la población celular que lo expresa.
Anotaciones
Referencias
enlaces externos
- Difteria + Toxina en los Encabezamientos de Materia Médica (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Cómo actúa la toxina diftérica - Animación


