Heptóxido de dicloro - Dichlorine heptoxide

|
|
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Heptóxido de dicloro
|
|
| Otros nombres
Óxido de cloro (VII); Anhídrido perclórico; (Percloriloxi) trióxido de clorano
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
|
PubChem CID
|
|
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| Cl 2 O 7 | |
| Masa molar | 182,901 g / mol |
| Apariencia | líquido incoloro |
| Densidad | 1,9 g / cm 3 |
| Punto de fusion | −91,57 ° C (−132,83 ° F; 181,58 K) |
| Punto de ebullición | 82 ° C (180 ° F; 355 K) |
| se hidroliza para formar ácido perclórico | |
| Peligros | |
| Principales peligros | oxidante, explosivo por contacto |
| NFPA 704 (diamante de fuego) | |
| Compuestos relacionados | |
|
Compuestos relacionados
|
Heptóxido de manganeso |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El heptóxido de dicloro es el compuesto químico con la fórmula Cl 2 O 7 . Este óxido de cloro es el anhídrido del ácido perclórico . Se produce mediante la cuidadosa destilación de ácido perclórico en presencia del agente deshidratante pentóxido de fósforo :
- 2 HClO 4 + P 4 O 10 → Cl 2 O 7 + H 2 P 4 O 11
El óxido de cloro (VII) se puede eliminar por destilación de la mezcla.
También puede formarse mediante iluminación sobre mezclas de cloro y ozono . Se hidroliza lentamente de nuevo a ácido perclórico , que también es peligroso cuando está anhidro .
Estructura
El Cl 2 O 7 es una molécula endergónica, lo que significa que es intrínsecamente inestable y se descompone en sus elementos constituyentes con la liberación de energía:
- 2 Cl 2 O 7 → 2 Cl 2 + 7 O 2 (Δ H ° = –132 kcal / mol)
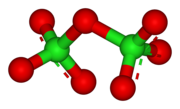
El Cl 2 O 7 se dobla con un ángulo de Cl − O − Cl de 118,6 °, lo que da a la molécula de simetría C 2 . Las distancias terminales Cl − O son 1.709 Å y las distancias Cl = O son 1.405 Å. En este compuesto, el cloro existe en su estado de oxidación formal más alto de +7, aunque el enlace en esta molécula es significativamente covalente.
Química
El heptóxido de dicloro reacciona con aminas primarias y secundarias en una solución de tetracloruro de carbono para producir amidas perclóricas:
- 2 RNH
2 + Cl
2 O
7 → 2 RNHClO
3 + H
2 O - 2 R
2 NH + Cl
2 O
7 → 2 R
2 NClO
3 + H
2 O
También reacciona con alquenos para dar alquil percloratos. Por ejemplo, reacciona con propeno en una solución de tetracloruro de carbono para producir perclorato de isopropilo y perclorato de 1-cloro-2-propilo.
El heptóxido de dicloro es un óxido fuertemente ácido y en solución forma un equilibrio con el ácido perclórico.
Seguridad
Aunque es el óxido de cloro más estable, el Cl 2 O 7 es un oxidante fuerte así como un explosivo que se puede detonar con llamas o golpes mecánicos, o por contacto con yodo . Sin embargo, es menos oxidante que los otros óxidos de cloro y no ataca el azufre , el fósforo o el papel cuando está frío. Tiene los mismos efectos en el cuerpo humano que el cloro elemental y requiere las mismas precauciones.

