Espectroscopía de rayos X de dispersión de longitud de onda - Wavelength-dispersive X-ray spectroscopy
| Acrónimo | WDXS WDS |
|---|---|
| Clasificación | Espectroscopia |
| Analitos | Elementos en sólidos, líquidos, polvos y películas delgadas |
| Fabricantes | Anton Paar , Bruker AXS , Hecus, Malvern Panalytical, Rigaku Corporation , Xenocs |
| Otras tecnicas | |
| Relacionados | espectroscopia de rayos X de energía dispersiva |
La espectroscopia de rayos X de dispersión de longitud de onda ( WDXS o WDS ) es una técnica de análisis no destructiva que se utiliza para obtener información elemental sobre una variedad de materiales midiendo los rayos X característicos dentro de un rango de longitud de onda pequeño. La técnica genera un espectro en el que los picos corresponden a líneas de rayos X específicas y los elementos pueden identificarse fácilmente. WDS se utiliza principalmente en el análisis químico, longitud de onda de dispersión de fluorescencia de rayos X (WDXRF) espectrometría , microsondas de electrones , el escaneo de microscopios electrónicos , y los experimentos de alta precisión para la prueba física atómica y plasma.
Teoría
La espectroscopia de rayos X de dispersión de longitud de onda se basa en principios conocidos de cómo los rayos X característicos son generados por una muestra y cómo se miden los rayos X.
Generación de rayos X
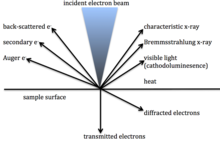
Los rayos X se generan cuando un haz de electrones de energía suficientemente alta desaloja un electrón de un orbital interno dentro de un átomo o ión, creando un vacío. Este vacío se llena cuando un electrón de un orbital superior libera energía y desciende para reemplazar el electrón desprendido. La diferencia de energía entre los dos orbitales es característica de la configuración electrónica del átomo o ión y puede usarse para identificar el átomo o ión.
Los elementos más ligeros, hidrógeno , helio , litio , berilio hasta el número atómico 5, no tienen electrones en los orbitales externos para reemplazar un electrón desplazado por el haz de electrones y, por lo tanto, no pueden detectarse utilizando esta técnica.
Medición de rayos X
De acuerdo con la ley de Bragg , cuando un haz de rayos X de longitud de onda "λ" golpea la superficie de un cristal en un ángulo "Θ" y el cristal tiene planos de retícula atómica separados por una distancia "d", la interferencia constructiva dará como resultado un haz de rayos X difractados que serán emitidos por el cristal en el ángulo "Θ" si
- nλ = 2d sin Θ, donde n es un número entero .
Esto significa que un cristal con un tamaño de celosía conocido desviará un haz de rayos X de un tipo específico de muestra en un ángulo predeterminado. El haz de rayos X se puede medir colocando un detector (generalmente un contador de centelleo o un contador proporcional ) en la trayectoria del haz desviado y, dado que cada elemento tiene una longitud de onda de rayos X distintiva, se pueden determinar varios elementos teniendo múltiples cristales y detectores múltiples.
Para mejorar la precisión, los haces de rayos X suelen colimarse mediante láminas de cobre paralelas llamadas colimador de Söller . El monocristal, la muestra y el detector se montan con precisión en un goniómetro con la distancia entre la muestra y el cristal igual a la distancia entre el cristal y el detector. Suele funcionar al vacío para reducir la absorción de radiación suave (fotones de baja energía) por el aire y así aumentar la sensibilidad para la detección y cuantificación de elementos ligeros (entre boro y oxígeno ). La técnica genera un espectro con picos correspondientes a líneas de rayos X. Esto se compara con los espectros de referencia para determinar la composición elemental de la muestra.
A medida que aumenta el número atómico del elemento, hay más electrones posibles a diferentes niveles de energía que pueden ser expulsados, lo que da como resultado rayos X con diferentes longitudes de onda. Esto crea espectros con múltiples líneas, una para cada nivel de energía. El pico más grande del espectro se denomina K α , el siguiente K β , y así sucesivamente.
Aplicaciones
Las aplicaciones incluyen análisis de catalizadores, cemento, alimentos, metales, minería y muestras minerales, petróleo, plásticos, semiconductores y madera.
Limitaciones
- El análisis generalmente se limita a un área muy pequeña de la muestra, aunque los equipos automatizados modernos a menudo usan patrones de cuadrícula para áreas de análisis más grandes.
- La técnica no puede distinguir entre isótopos de elementos ya que la configuración electrónica de los isótopos de un elemento es idéntica.
- No puede medir el estado de valencia del elemento, por ejemplo Fe 2+ vs Fe 3+ .
- En ciertos elementos, la línea K α podría superponerse a la K β de otro elemento y, por lo tanto, si el primer elemento está presente, el segundo elemento no se puede detectar de manera confiable (por ejemplo, V K α se superpone a Ti K β )