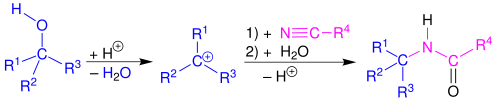Reacción de Ritter - Ritter reaction
| Reacción de Ritter | |
|---|---|
| Lleva el nombre de | John J. Ritter |
| Tipo de reacción | Reacción de adición |
| Identificadores | |
| Portal de química orgánica | reacción-ritter |
| ID de ontología RSC | RXNO: 0000058 |
La reacción de Ritter es una reacción química que transforma un nitrilo en una N -alquil amida utilizando varios reactivos alquilantes electrofílicos . La reacción original formó el agente alquilante usando un alqueno en presencia de un ácido fuerte .
Mecanismo y alcance
La reacción de Ritter procede mediante la adición electrofílica de un ión carbenio o especies covalentes al nitrilo . El ion nitrilo resultante se hidroliza con agua a la amida deseada.
Los alcoholes primarios, secundarios, terciarios y bencílicos , así como el acetato de terc- butilo, también reaccionan con éxito con nitrilos en presencia de ácidos fuertes para formar amidas mediante la reacción de Ritter. Se puede utilizar una amplia gama de nitrilos. En particular, se puede usar formonitrilo (cianuro de hidrógeno) para preparar formamidas, que son precursores útiles de los isocianuros.
Aplicaciones
La aplicación a gran escala de la reacción de Ritter se encuentra en la síntesis de terc-octilamina . De esta forma se preparan unas 10.000 toneladas / año (año 2000) de esta y otras aminas lipofílicas relacionadas. De lo contrario, la reacción de Ritter es más útil en la formación de aminas y amidas de interés farmacéutico. Las aplicaciones del mundo real incluyen la síntesis a escala industrial de Merck del fármaco anti- VIH Crixivan (indinavir); la producción del inhibidor de falcipaína-2 PK-11195 ; la síntesis del alcaloide aristotelona; y síntesis de amantadina , un fármaco antivírico y antiparkinsoniano. Otras aplicaciones de la reacción de Ritter incluyen la síntesis de ligandos del receptor de dopamina y la producción lícita e ilícita de anfetamina racémica a partir de alilbenceno y cianuro de metilo .
La reacción de Ritter es inferior a la mayoría de los métodos de aminación porque cogenera cantidades sustanciales de sales. Es ilustrativa la conversión de isobutileno en terc-butilamina usando HCN y ácido sulfúrico seguido de neutralización básica. El peso del subproducto de la sal es mayor que el peso de la amina.
En el laboratorio, la reacción de Ritter adolece de la necesidad de un catalizador ácido extremadamente fuerte . Se han propuesto otros métodos para promover la formación de carbocatión , incluida la transferencia de electrones fotocatalíticos o la fotólisis directa.
Historia
La reacción lleva el nombre de John J. Ritter, quien supervisó el Ph.D. trabajo de tesis de P. Paul Minieri .
- Ritter, John J .; Minieri, P. Paul (1948). "Una nueva reacción de nitrilos. I. Amidas de alquenos y mononitrilos". Revista de la Sociedad Química Estadounidense . 70 (12): 4045–8. doi : 10.1021 / ja01192a022 . PMID 18105932 .
- Ritter, John J .; Kalish, Joseph (1948). "Una nueva reacción de nitrilos. II. Síntesis de t -carbinaminas". Revista de la Sociedad Química Estadounidense . 70 (12): 4048–50. doi : 10.1021 / ja01192a023 . PMID 18105933 .
- Zil'berman, EN (1960). "Algunas reacciones de los nitrilos con la formación de un nuevo enlace nitrógeno-carbono". Reseñas de productos químicos rusos . 29 (6): 331–340. Código Bibliográfico : 1960RuCRv..29..331Z . doi : 10.1070 / RC1960v029n06ABEH001235 .