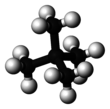
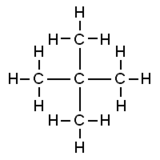
Neopentano - Neopentane

|
|||
|
|||
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
2,2-dimetilpropano |
|||
| Otros nombres
Neopentano
tetrametilmetano |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 1730722 | |||
| CHEBI | |||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.006.677 |
||
| Número CE | |||
| 1850 | |||
| Malla | neopentano | ||
|
PubChem CID
|
|||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 5 H 12 | |||
| Masa molar | 72,151 g · mol −1 | ||
| Apariencia | Gas incoloro | ||
| Olor | Inodoro | ||
| Densidad | 3.255 kg / m 3 (gas, 9.5 ° C) 601.172 kg / m 3 (líquido, 9.5 ° C) |
||
| Punto de fusion | −16,5 ° C (2,3 ° F; 256,6 K) | ||
| Punto de ebullición | 9,5 ° C (49,1 ° F; 282,6 K) | ||
| Presión de vapor | 146 kPa (a 20 ° C) | ||
|
Constante de la ley de Henry ( k H ) |
4,7 nmol Pa −1 kg −1 | ||
| Termoquímica | |||
|
Capacidad calorífica ( C )
|
121.07–120.57 JK −1 mol −1 | ||
|
Entropía molar estándar ( S |
217 JK −1 mol −1 | ||
| −168,5–−167,3 kJ mol −1 | |||
| −3,51506–−3,51314 MJ mol −1 | |||
| Riesgos | |||
|
|
|||
| Frases R (desactualizadas) | R12 , R51 / 53 | ||
| Frases S (desactualizadas) | (S2) , S16 , S33 | ||
| NFPA 704 (diamante de fuego) | |||
| Compuestos relacionados | |||
|
Alcanos relacionados
|
|||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El neopentano , también llamado 2,2-dimetilpropano , es un alcano de cadena doble ramificada con cinco átomos de carbono . El neopentano es un gas inflamable a temperatura y presión ambiente que puede condensarse en un líquido altamente volátil en un día frío, en un baño de hielo o cuando se comprime a una presión más alta.
El neopentano es el alcano más simple con un carbono cuaternario y tiene simetría tetraédrica aquiral . Es uno de los tres isómeros estructurales con la fórmula molecular C 5 H 12 ( pentanos ), siendo los otros dos n -pentano e isopentano . De estos tres, es el único que es un gas en condiciones estándar; los otros son líquidos.
Nomenclatura
El nombre tradicional neopentano todavía se mantuvo en las recomendaciones de la IUPAC de 1993 , pero ya no se recomienda de acuerdo con las recomendaciones de 2013. El nombre preferido de la IUPAC es el nombre sistemático 2,2-dimetilpropano, pero los números de los sustituyentes son superfluos porque es el único "dimetilpropano" posible.
Un sustituyente neopentilo , a menudo simbolizado por "Np", tiene la estructura Me 3 C – CH 2 , por ejemplo, alcohol neopentílico (Me 3 CCH 2 OH o NpOH). Como Np también simboliza el elemento neptunio (número atómico 93), se debe usar esta abreviatura con cuidado.
También se utiliza el nombre obsoleto tetrametilmetano, especialmente en fuentes más antiguas.
Propiedades físicas
Puntos de ebullición y fusión
El punto de ebullición del neopentano es de solo 9,5 ° C, significativamente más bajo que el del isopentano (27,7 ° C) y el pentano normal (36,0 ° C). Por lo tanto, el neopentano es un gas a temperatura ambiente y presión atmosférica, mientras que los otros dos isómeros son (apenas) líquidos.
El punto de fusión del neopentano (−16,6 ° C), por otro lado, es 140 grados más alto que el del isopentano (−159,9 ° C) y 110 grados más alto que el del n -pentano (−129,8 ° C). Esta anomalía se ha atribuido al mejor empaquetamiento en estado sólido que se supone es posible con la molécula tetraédrica de neopentano; pero esta explicación ha sido cuestionada debido a que tiene una densidad más baja que los otros dos isómeros. Además, su entalpía de fusión es menor que las entalpías de fusión tanto del n -pentano como del isopentano, lo que indica que su alto punto de fusión se debe a un efecto de entropía resultante de una simetría molecular superior. De hecho, la entropía de fusión del neopentano es aproximadamente cuatro veces menor que la del n -pentano y el isopentano.
1 H RMN espectro
Debido a la simetría tetraédrica completa del neopentano , todos los protones son químicamente equivalentes, lo que lleva a un solo desplazamiento químico de RMN δ = 0,902 cuando se disuelven en tetracloruro de carbono . A este respecto, el neopentano es similar a su análogo de silano , el tetrametilsilano , cuyo único desplazamiento químico es cero por convención.
La simetría de la molécula de neopentano se puede romper si algunos átomos de hidrógeno se reemplazan por átomos de deuterio . En particular, si cada grupo metilo tiene un número diferente de átomos sustituidos (0, 1, 2 y 3), se obtiene una molécula quiral . La quiralidad en este caso surge únicamente por la distribución de masa de sus núcleos, mientras que la distribución de electrones sigue siendo esencialmente aquiral.
Referencias
enlaces externos
- Linstrom, Peter J .; Mallard, William G. (eds.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69 , National Institute of Standards and Technology, Gaithersburg (MD), http://webbook.nist.gov
- Nomenclatura de Química Orgánica de la IUPAC (versión en línea del " Libro Azul ")