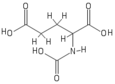
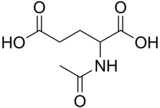
Ácido N- acetilglutámico - N-Acetylglutamic acid
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Ácido 2-acetamidopentanodioico
|
|
| Otros nombres
Ácido acetilglutámico
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 3DMet | |
| Abreviaturas | |
| 1727473 S | |
| CHEBI | |
| ChemSpider | |
| DrugBank | |
| Tarjeta de información ECHA |
100.024.899 |
| Número CE | |
| KEGG | |
| Malla | N-acetilglutamato |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
|
|
|
| Propiedades | |
| C 7 H 11 N O 5 | |
| Masa molar | 189,167 g · mol −1 |
| Apariencia | Cristales blancos |
| Densidad | 1 g mL −1 |
| Punto de fusion | 191 a 194 ° C (376 a 381 ° F; 464 a 467 K) |
| 36 g L −1 | |
| Riesgos | |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis media )
|
> 7 g kg -1 (oral, rata) |
| Compuestos relacionados | |
|
Ácidos alcanoicos relacionados
|
|
|
Compuestos relacionados
|
|
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El ácido N- acetilglutamato (también conocido como N- acetilglutamato , abreviado NAG , fórmula química C 7 H 11 NO 5 ) se biosintetiza a partir de glutamato y acetilornitina por la ornitina acetiltransferasa, y del ácido glutámico y acetil-CoA por la enzima N -acetil-CoA por la enzima N- acetilglutamato. . La reacción inversa, la hidrólisis del grupo acetilo, es catalizada por una hidrolasa específica. Es el primer intermediario involucrado en la biosíntesis de arginina en procariotas y eucariotas simples y un regulador en el proceso conocido como ciclo de la urea que convierte el amoníaco tóxico en urea para su excreción del cuerpo en vertebrados.
Descubrimiento
El ácido N- acetilglutámico es un metabolito extracelular aislado del procariota Rhizobium trifolii que se caracterizó utilizando muchas técnicas de determinación de la estructura, como la espectroscopia de resonancia magnética nuclear de protones ( 1 H RMN), la espectroscopia de infrarrojos por transformada de Fourier y la cromatografía de gases y la espectrometría de masas .
En Rhizobium , la acumulación extracelular de ácido N- acetilglutámico se debe al metabolismo que involucra genes del factor nod en un plásmido simbiótico . Cuando se mutan los factores de nod, se produce menos ácido N- acetilglutaámico.
Biosíntesis
Procariotas y eucariotas simples
En procariotas y eucariotas simples, el ácido N- acetilglutámico puede ser producido por N- acetilglutamato sintasa (NAGS) u ornitina acetiltransferasa (OAT).
Síntesis de ornitina acetiltransferasa (OAT)
OAT sintetiza ácido N- acetilglutámico a partir de glutamato y acetilornitina y es el método de elección para la producción en procariotas que tienen la capacidad de sintetizar el compuesto ornitina .
Síntesis de N- acetilglutamato sintasa (NAGS)
La N- acetilglutamato sintasa es una enzima que sirve como reforzador del ácido N- acetilglutámico para complementar cualquier ácido N- acetilglutámico perdido por la célula a través de la mitosis o degradación. NAGS sintetiza ácido N- acetilglutámico catalizando la adición de un grupo acetilo de la acetil-coenzima A al glutamato . En procariotas con producción de ornitina no cíclica, NAGS es el único método de síntesis del ácido N- acetilglutaámico y es inhibido por la arginina. Se cree que la acetilación del glutamato evita que el glutamato sea utilizado por la biosíntesis de prolina .
Vertebrados
A diferencia de los procariotas, la NAGS en los mamíferos se ve reforzada por la arginina, junto con las protaminas . Es inhibido por el ácido N- acetilglutámico y sus análogos (otros compuestos N -acetilados).
El cerebro también contiene ácido N- acetilglutámico en cantidades mínimas, sin embargo, no se encuentra expresión de NAGS. Esto sugiere que el ácido N- acetilglutámico es producido por otra enzima en el cerebro que aún no se ha determinado.
Roles biológicos
Vertebrados y mamíferos
En vértebras y mamíferos, el ácido N- acetilglutámico es la molécula activadora alostérica de la carbamil fosfato sintetasa I mitocondrial (CPSI), que es la primera enzima del ciclo de la urea. Desencadena la producción del primer intermedio del ciclo de la urea, carbamil fosfato . La CPSI está inactiva cuando no está presente el ácido N- acetilglutámico. En el hígado y el intestino delgado, el CPSI dependiente del ácido N- acetilglutámico produce citrulina , el segundo intermedio en el ciclo de la urea. La distribución del ácido N- acetilglutámico en las células hepáticas es máxima en las mitocondrias con un 56% de la disponibilidad total de ácido N- acetilglutámico, un 24% en el núcleo y el 20% restante en el citosol. La aminoacilasa I en las células hepáticas y renales degrada el ácido N- acetilglutámico en glutamato y acetato. Por el contrario, el ácido N- acetilglutámico no es el cofactor alostérico de la carbamil fosfato sintetasa que se encuentra en el citoplasma, que participa en la síntesis de pirimidina .
Las concentraciones de ácido N- acetilglutámico aumentan cuando aumenta el consumo de proteínas debido a la acumulación de amoníaco que debe secretarse a través del ciclo de la urea, lo que respalda el papel del ácido N- acetilglutámico como cofactor de CPSI. Además, el ácido N- acetilglutámico se puede encontrar en muchos alimentos de consumo común como la soja, el maíz y el café, y el cacao en polvo contiene una concentración notablemente alta.
La deficiencia de ácido N- acetilglutámico en humanos es un trastorno autosómico recesivo que produce un bloqueo de la producción de urea que finalmente aumenta la concentración de amoníaco en la sangre ( hiperamonemia ). La deficiencia puede ser causada por defectos en el gen que codifica NAGS o por deficiencias en los precursores esenciales para la síntesis.
Bacterias
El ácido N- acetilglutámico es el segundo intermedio en la vía de producción de arginina en Escherichia coli y se produce a través de NAGS. En esta vía, la quinasa del ácido N- acetilglutámico (NAGK) cataliza la fosforilación del grupo gamma (tercer) carboxilo del ácido N- acetilglutámico utilizando el fosfato producido por hidrólisis de trifosfato de adenosina (ATP).
Raíces de plántulas de trébol blanco
Rhizobium puede formar una relación simbiótica con las raíces de las plántulas de trébol blanco y formar colonias. El ácido N- acetilglutámico extracelular producido por estas bacterias tiene tres efectos morfológicos en las raíces de las plántulas del trébol blanco: ramificación de los pelos de las raíces, hinchazón de las puntas de las raíces y aumento del número de divisiones celulares en las células indiferenciadas que se encuentran en la capa celular más externa. de la raíz. Esto sugiere que el ácido N- acetilglutámico está involucrado en la estimulación de la mitosis. Se observaron los mismos efectos en el trébol de fresa , pero no en las legumbres . Los efectos del ácido N- acetilglutámico en las especies de trébol fueron más potentes que los efectos de la glutamina , glutamato, arginina o amoníaco .
Estructura
El ácido N- acetilglutámico está compuesto por dos grupos de ácido carboxílico y un grupo amida que sobresale del segundo carbono. La estructura del ácido N- acetilglutámico a pH fisiológico (7,4) tiene todos los grupos carboxilo desprotonados .
Espectroscopia de RMN de protones
La estructura molecular del ácido N- acetilglutámico se determinó usando espectroscopía de RMN de protón . La RMN de protones revela la presencia y la ubicación del grupo funcional de los protones en función de los cambios químicos registrados en el espectro.
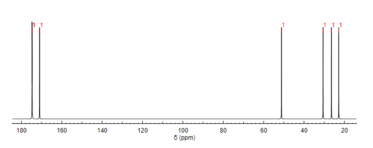
13 espectroscopia de RMN de C
Como RMN de protón, carbono-13 ( 13 C) espectroscopia RMN es un método utilizado en la determinación de la estructura molecular. La 13C NMR revela los tipos de carbonos presentes en una molécula en función de los cambios químicos que corresponden a ciertos grupos funcionales. El ácido N- acetilglutámico exhibe carbonilos de carbonilo de manera más distintiva debido a los tres sustituyentes que contienen carbonilo.