Bicarbonato de magnesio - Magnesium bicarbonate
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Hidrogenocarbonato de magnesio
|
|
| Otros nombres
Bicarbonato de magnesio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.016.582 |
| Número CE | |
| Número e | E504 (ii) (reguladores de acidez, ...) |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
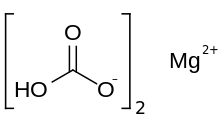
| Mg (HCO 3 ) 2 | |
| Masa molar | 146,34 g / mol |
| 0,077 g / (100 ml) | |
| Compuestos relacionados | |
|
Otros cationes
|
Bicarbonato de calcio |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El bicarbonato de magnesio o bicarbonato de magnesio , Mg ( H CO 3 ) 2 , es la sal de bicarbonato de magnesio . Puede formarse mediante la reacción de soluciones diluidas de ácido carbónico (como agua mineral ) e hidróxido de magnesio (leche de magnesia).
Se puede preparar mediante la síntesis de acetato de magnesio y bicarbonato de sodio Mg (CH3COO) 2 + 2NaHCO3 = Mg (HCO3) 2 + 2CH3COONa
El bicarbonato de magnesio existe solo en solución acuosa. El magnesio no forma bicarbonato sólido como el litio. Para producirlo, se trata una suspensión de hidróxido de magnesio con dióxido de carbono presurizado , produciendo una solución de bicarbonato de magnesio:
- Mg (OH) 2 + 2 CO 2 → Mg (HCO 3 ) 2
El secado de la solución resultante hace que el bicarbonato de magnesio se descomponga , produciendo carbonato de magnesio , dióxido de carbono y agua:
- Mg 2+ + 2 HCO 3 - → MgCO 3 + CO 2 + H 2 O
