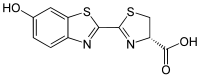
Luciferina de luciérnaga - Firefly luciferin
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Ácido (4 S ) -2- (6-hidroxi-1,3-benzotiazol-2-il) -4,5-dihidrotiazol-4-carboxílico
|
|
| Otros nombres
D - (-) - Luciferina, luciferina de escarabajo
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.018.166 |
| Número CE | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 11 H 8 N 2 O 3 S 2 | |
| Masa molar | 280,32 g · mol −1 |
| UV-vis (λ máx. ) | 330 nm (soluciones acuosas neutras y algo ácidas) |
| Absorbancia | ε 330 = 18,2 mM −1 cm −1 |
| Riesgos | |
| Pictogramas GHS |

|
| Palabra de señal GHS | Advertencia |
| H315 , H319 , H335 | |
| P261 , P264 , P271 , P280 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 | |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
| Referencias de Infobox | |
Luciferina de luciérnaga (también conocida como luciferina de escarabajo ) es la luciferina , o compuesto emisor de luz, que se utiliza para los sistemas bioluminiscentes de luciérnaga ( Lampyridae ), gusano de ferrocarril ( Phengodidae ), gusano de estrella ( Rhagophthalmidae ) y escarabajo de clic ( Pyrophorini ). Es el sustrato de la luciferasa ( EC 1.13.12.7), responsable de la característica emisión de luz amarilla de muchas especies de luciérnagas .
Como ocurre con todas las demás luciferinas, se requiere oxígeno para generar luz; sin embargo, también se ha encontrado que el trifosfato de adenosina (ATP) y el magnesio son necesarios para la emisión de luz.
Historia
Gran parte del trabajo inicial sobre la química de la luminiscencia de las luciérnagas se realizó en el laboratorio de William D. McElroy en la Universidad Johns Hopkins . La luciferina se aisló y purificó por primera vez en 1949, aunque pasarían varios años hasta que se desarrollara un procedimiento para cristalizar el compuesto con alto rendimiento. Esto, junto con la síntesis y elucidación de la estructura, fue logrado por el Dr. Emil H. White en el Departamento de Química de la Universidad Johns Hopkins. El procedimiento fue una extracción ácido-base , dado el grupo ácido carboxílico en la luciferina. La luciferina podría extraerse eficazmente utilizando acetato de etilo a pH bajo a partir de polvo de aproximadamente 15.000 linternas de luciérnagas. La estructura se confirmó más tarde mediante el uso combinado de espectroscopía infrarroja , espectroscopía UV-vis y métodos sintéticos para degradar el compuesto en fragmentos identificables.
Propiedades
Se encontró que la luciferina cristalina es fluorescente , absorbe luz ultravioleta con un pico a 327 nm y emite luz con un pico a 530 nm. La emisión visible se produce tras la relajación de la oxiluciferina desde un estado excitado singlete hasta su estado fundamental. Las soluciones alcalinas provocaron un corrimiento al rojo de la absorción probablemente debido a la desprotonación del grupo hidroxilo en el benzotiazol , pero no afectaron la emisión de fluorescencia. Se encontró que el adenilato de luciferilo (el éster AMP de luciferina) emite luz de forma espontánea en solución. Las diferentes especies de luciérnagas usan la misma luciferina, sin embargo, el color de la luz emitida puede diferir mucho. Se midió que la luz de Photuris pennsylvanica era de 552 nm (verde-amarillo) mientras que se midió que Pyrophorus plagiophthalamus emitía luz a 582 nm (naranja) en el órgano ventral. Es probable que tales diferencias se deban a cambios de pH o diferencias en la estructura primaria de la luciferasa. La modificación del sustrato de luciferina de luciérnaga ha dado lugar a emisiones "desplazadas al rojo" (hasta una longitud de onda de emisión de 675 nm).
Actividad biológica
La síntesis in vivo de luciferina de luciérnaga no se comprende completamente. Solo se ha estudiado el paso final de la vía enzimática, que es la reacción de condensación de D - cisteína con 2-ciano-6-hidroxibenzotiazol , y es la misma reacción que se utiliza para producir el compuesto de forma sintética. Esto se confirmó mediante el radiomarcaje de átomos en los dos compuestos y mediante la identificación de una enzima regeneradora de luciferina .
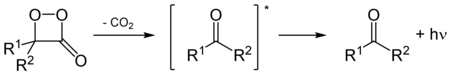
En la luciérnaga , la oxidación de luciferinas, que es catalizada por luciferasas, produce un peroxi compuesto 1,2-dioxetano . El dioxetano es inestable y se descompone espontáneamente en dióxido de carbono y cetonas excitadas , que liberan el exceso de energía al emitir luz ( bioluminiscencia ).
La luciferina de luciérnaga y los sustratos modificados son imitadores de ácidos grasos y se han utilizado para localizar la amida hidrolasa de ácidos grasos (FAAH) in vivo. La luciferina de luciérnaga es un sustrato del transportador ABCG2 y se ha utilizado como parte de un ensayo de alto rendimiento de imágenes de bioluminiscencia para detectar inhibidores del transportador.
Referencias
enlaces externos
- Página de bioluminiscencia que muestra los principales tipos de luciferina