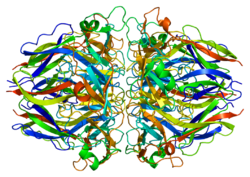
Colágeno, tipo IV, alfa 1 - Collagen, type IV, alpha 1
La cadena de colágeno alfa-1 (IV) (COL4A1) es una proteína que en los seres humanos está codificada por el gen COL4A1 en el cromosoma 13 . Se expresa de forma ubicua en muchos tejidos y tipos de células. COL4A1 es una subunidad del colágeno tipo IV y juega un papel en la angiogénesis . Las mutaciones en el gen se han relacionado con enfermedades del cerebro , los músculos , los riñones , los ojos y el sistema cardiovascular . El gen COL4A1 también contiene uno de los 27 SNP asociados con un mayor riesgo de enfermedad de las arterias coronarias .
Estructura
Gene
El gen COL4A1 reside en el cromosoma 13 en la banda 13q34 y contiene 54 exones . [5] Este gen produce 2 isoformas mediante un empalme alternativo .
Proteína
COL4A1 pertenece a la familia del colágeno tipo IV y contiene tres dominios: un dominio N-terminal corto , un dominio 7S de triple hélice largo en su centro y un dominio 1 no colágeno (NC1) en su C-terminal . El dominio de triple hélice contiene repeticiones GXY interrumpidas, que se sospecha que permiten la flexibilidad del dominio. El dominio NC1 está compuesto por dos tapas triméricas, cada una de las cuales contiene dos fragmentos alfa 1 y un fragmento alfa 2, que forman una hélice séxtuple dispuesta alrededor de un túnel axial. La interacción entre estos dos casquetes se produce a lo largo de una gran interfaz plana y se estabiliza mediante un entrecruzamiento covalente entre las cadenas alfa 1 y alfa 2 a través de los dos casquetes.
Función
El colágeno tipo IV es el principal componente estructural de las membranas basales , que contiene dos o tres proteínas COL4A1. Por tanto, COL4A1 es abundante y se encuentra en todo tipo de membranas basales. El dominio NC1 de COL4A1 es una molécula antiangiogénica importante para controlar la formación de nuevos capilares . NC1 se une a la integrina α1β1 e inhibe las vías de señalización de integrinas específicas en las células epiteliales vasculares. También regula la expresión de HIF-1α y VEGF , presumiblemente inhibiendo la cascada de señalización de MAPK . Estos hallazgos pueden explicar la función antitumoral de NC1.
Significación clínica
Las mutaciones en COL4A1 exones 24 y 25 están asociados con Hanac ( autosómica dominante hereditaria angiopatía con nefropatía , aneurismas , y calambres musculares ). También se ha confirmado que las mutaciones en el gen COL4A1 ocurren en algunos pacientes con porencefalia y esquizencefalia .
En los seres humanos, se descubrió que una nueva mutación del gen COL4A1 que codifica el colágeno tipo IV está asociada con la catarata congénita autosómica dominante en una familia china. Esta mutación no se encontró en miembros de la familia no afectados ni en 200 controles no relacionados. En este estudio, el análisis de secuencia confirmó que el residuo de aminoácido Gly782 estaba altamente conservado. Este informe de una nueva mutación en el gen COL4A1 es el primer informe de una catarata congénita autosómica dominante no sindrómica que destaca un papel importante del colágeno tipo IV en las propiedades fisiológicas y ópticas del cristalino.
Además, en el campo cardiovascular, las regiones COL4A1 y COL4A2 en el cromosoma 13q34 son un locus altamente replicado para la enfermedad de las arterias coronarias. En una pared normal de arterias, el colágeno tipo IV actúa para inhibir la proliferación de células de músculo liso. Por consiguiente, se demostró que la expresión de la proteína del colágeno tipo IV en las células del músculo liso vascular humano está regulada por la estimulación del ARNm mediada tanto por la proteína SMAD3 como por el TGFβ. En conjunto, se concluyó que la patogenia de la enfermedad de las arterias coronarias puede estar regulada por los genes COL4A1 y COL4A2.
También se ha informado de una encefalopatía autosómica recesiva asociada con mutaciones en este gen.
Marcador clínico
Un estudio de puntuación de riesgo genético de múltiples locus basado en una combinación de 27 loci, incluido el gen COL4A1, identificó individuos con mayor riesgo de eventos de enfermedad arterial coronaria tanto incidentes como recurrentes, así como un beneficio clínico mejorado de la terapia con estatinas. El estudio se basó en un estudio de cohorte comunitario (el estudio Malmo Diet and Cancer) y cuatro ensayos controlados aleatorios adicionales de cohortes de prevención primaria (JUPITER y ASCOT) y cohortes de prevención secundaria (CARE y PROVE IT-TIMI 22).
Referencias
Otras lecturas
- Tryggvason K, Soininen R, Hostikka SL, Ganguly A, Huotari M, Prockop DJ (1990). "Estructura de los genes del colágeno humano tipo IV". Anales de la Academia de Ciencias de Nueva York . 580 : 97-111. doi : 10.1111 / j.1749-6632.1990.tb17922.x . PMID 2186699 . S2CID 44878809 .
- Hinek A (julio de 1994). "Naturaleza y las múltiples funciones de la proteína de unión de elastina / laminina de 67 kD". Adhesión y comunicación celular . 2 (3): 185–93. doi : 10.3109 / 15419069409004436 . PMID 7827955 .
- Ständer M, Naumann U, Wick W, Weller M (mayo de 1999). "Transformación del factor de crecimiento beta y p-21: múltiples dianas moleculares de la supresión del crecimiento neoplásico mediada por decorina". Investigación de células y tejidos . 296 (2): 221–7. doi : 10.1007 / s004410051283 . PMID 10382266 . S2CID 20282995 .
- Kurpakus Wheater M, Kernacki KA, Hazlett LD (mayo de 1999). "Proteínas de las células corneales y patología de la superficie ocular". Biotecnología e histoquímica . 74 (3): 146–59. doi : 10.3109 / 10520299909047967 . PMID 10416788 .
- Ghebrehiwet B, Peerschke EI, Hong Y, Munoz P, Gorevic PD (junio de 1992). "Las secuencias cortas de aminoácidos derivadas del receptor C1q (C1q-R) muestran homología con las cadenas alfa de los receptores de fibronectina y vitronectina y del colágeno tipo IV". Revista de biología de leucocitos . 51 (6): 546–56. doi : 10.1002 / jlb.51.6.546 . PMID 1377218 . S2CID 1214598 .
- Gupta S, Batchu RB, Datta K (octubre de 1991). "Purificación, caracterización parcial de la proteína de unión al ácido hialurónico de riñón de rata y su localización en la superficie celular". Revista europea de biología celular . 56 (1): 58–67. PMID 1724753 .
- Paralkar VM, Nandedkar AK, Pointer RH, Kleinman HK, Reddi AH (octubre de 1990). "Interacción de la osteogenina, una proteína morfogenética ósea que se une a la heparina, con el colágeno tipo IV" . La Revista de Química Biológica . 265 (28): 17281–4. doi : 10.1016 / S0021-9258 (17) 44900-3 . PMID 2211625 .
- Hernandez MR, Igoe F, Neufeld AH (agosto de 1986). "Matriz extracelular de la cabeza del nervio óptico humano". Revista Estadounidense de Oftalmología . 102 (2): 139–48. doi : 10.1016 / 0002-9394 (86) 90134-0 . PMID 2426947 .
- Aumailley M, Wiedemann H, Mann K, Timpl R (septiembre de 1989). "Unión de nidogen y el complejo laminina-nidogen al colágeno de membrana basal tipo IV" . Revista europea de bioquímica / FEBS . 184 (1): 241–8. doi : 10.1111 / j.1432-1033.1989.tb15013.x . PMID 2506015 .
- Pihlajaniemi T, Tryggvason K, Myers JC, Kurkinen M, Lebo R, Cheung MC, Prockop DJ, Boyd CD (junio de 1985). "Los clones de ADNc que codifican la cadena pro-alfa1 (IV) del procolágeno de tipo IV humano revelan una homología inusual de secuencias de aminoácidos en dos mitades del dominio carboxilo-terminal" . La Revista de Química Biológica . 260 (12): 7681–7. doi : 10.1016 / S0021-9258 (17) 39662-X . PMID 2581969 .
- Brinker JM, Gudas LJ, Loidl HR, Wang SY, Rosenbloom J, Kefalides NA, Myers JC (junio de 1985). "Homología restringida entre alfa 1 humano tipo IV y otras cadenas de procolágeno" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 82 (11): 3649–53. doi : 10.1073 / pnas.82.11.3649 . PMC 397843 . PMID 2582422 .
- Soininen R, Huotari M, Ganguly A, Prockop DJ, Tryggvason K (agosto de 1989). "Organización estructural del gen de la cadena alfa 1 del colágeno tipo IV humano" . La Revista de Química Biológica . 264 (23): 13565–71. doi : 10.1016 / S0021-9258 (18) 80034-5 . PMID 2701944 .
- Siebold B, Deutzmann R, Kühn K (octubre de 1988). "La disposición de enlaces disulfuro intra e intermoleculares en el dominio carboxiterminal, no colágeno de agregación y reticulación del colágeno de tipo IV de la membrana basal". Revista europea de bioquímica / FEBS . 176 (3): 617–24. doi : 10.1111 / j.1432-1033.1988.tb14321.x . PMID 2844531 .
- Pöschl E, Pollner R, Kühn K (septiembre de 1988). "Los genes de las cadenas alfa 1 (IV) y alfa 2 (IV) del colágeno tipo IV de la membrana basal humana están dispuestos uno al lado del otro y separados por un promotor bidireccional de estructura única" . El diario EMBO . 7 (9): 2687–95. doi : 10.1002 / j.1460-2075.1988.tb03122.x . PMC 457057 . PMID 2846280 .
- Bowcock AM, Hebert JM, Christiano AM, Wijsman E, Cavalli-Sforza LL, Boyd CD (1988). "El gen del colágeno pro alfa 1 (IV) está vinculado al locus D13S3 en el extremo distal del cromosoma humano 13q". Citogenética y Genética Celular . 45 (3–4): 234–6. doi : 10.1159 / 000132460 . PMID 2891465 .
- Solomon E, Hiorns LR, Spurr N, Kurkinen M, Barlow D, Hogan BL, Dalgleish R (mayo de 1985). "Asignaciones cromosómicas de los genes que codifican el colágeno humano de tipos II, III y IV: una familia de genes dispersos" . Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 82 (10): 3330–4. doi : 10.1073 / pnas.82.10.3330 . PMC 397769 . PMID 2987919 .
- Soininen R, Huotari M, Hostikka SL, Prockop DJ, Tryggvason K (noviembre de 1988). "Los genes estructurales de las cadenas alfa 1 y alfa 2 del colágeno de tipo IV humano están codificados de forma divergente en cadenas de ADN opuestas y tienen una región promotora superpuesta" . La Revista de Química Biológica . 263 (33): 17217–20. doi : 10.1016 / S0021-9258 (19) 77818-1 . PMID 3182844 .
- Brazel D, Oberbäumer I, Dieringer H, Babel W, Glanville RW, Deutzmann R, Kühn K (noviembre de 1987). "La finalización de la secuencia de aminoácidos de la cadena alfa 1 del colágeno de la membrana basal humana (tipo IV) revela 21 interrupciones no triples ubicadas dentro del dominio colágeno". Revista europea de bioquímica / FEBS . 168 (3): 529–36. doi : 10.1111 / j.1432-1033.1987.tb13450.x . PMID 3311751 .