Trióxido de boro - Boron trioxide
![Estructura cristalina de B2O3 [1]](https://upload.wikimedia.org/wikipedia/commons/thumb/d/d9/B2O3powder.JPG/220px-B2O3powder.JPG)
|
|
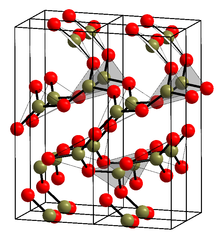
|
|
| Nombres | |
|---|---|
| Otros nombres
óxido de boro, trióxido de diboro, sesquióxido de boro, óxido bórico, boria
Anhídrido de ácido bórico |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.013.751 |
| Número CE | |
| 11108 | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| B 2 O 3 | |
| Masa molar | 69,6182 g / mol |
| Apariencia | blanco, sólido vidrioso |
| Densidad | 2,460 g / cm 3 , líquido; 2,55 g / cm 3 , trigonal; |
| Punto de fusion | 450 ° C (842 ° F; 723 K) (trigonal) 510 ° C (tetraédrico) |
| Punto de ebullición | 1.860 ° C (3.380 ° F; 2.130 K), sublima a 1500 ° C |
| 1,1 g / 100 ml (10 ° C) 3,3 g / 100 ml (20 ° C) 15,7 g / 100 ml (100 ° C) |
|
| Solubilidad | parcialmente soluble en metanol |
| Acidez (p K a ) | ~ 4 |
| -39,0 · 10 −6 cm 3 / mol | |
| Termoquímica | |
|
Capacidad calorífica ( C )
|
66,9 J / mol K |
|
Entropía molar estándar ( S |
80,8 J / mol K |
| -1254 kJ / mol | |
|
Energía libre de Gibbs (Δ f G ˚)
|
-832 kJ / mol |
| Riesgos | |
| Principales peligros | Irritante |
| Ficha de datos de seguridad | Ver: página de datos |
| Pictogramas GHS |

|
| Palabra de señal GHS | Peligro |
| H360FD | |
| P201 , P202 , P281 , P308 + 313 , P405 , P501 | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | incombustible |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis mediana )
|
3163 mg / kg (oral, ratón) |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
TWA 15 mg / m 3 |
|
REL (recomendado)
|
TWA 10 mg / m 3 |
|
IDLH (peligro inmediato)
|
2000 mg / m 3 |
| Página de datos complementarios | |
|
Índice de refracción ( n ), constante dieléctrica (ε r ), etc. |
|
|
Datos termodinámicos |
Comportamiento de fase sólido-líquido-gas |
| UV , IR , RMN , MS | |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El trióxido de boro (o trióxido de diboro ) es uno de los óxidos de boro . Es un sólido vítreo blanco con la fórmula B 2 O 3 . Casi siempre se encuentra en forma vítrea (amorfa); sin embargo, puede cristalizarse después de un recocido extenso (es decir, bajo calor prolongado).
Se cree que el óxido de boro vítreo (gB 2 O 3 ) está compuesto por anillos de boroxol que son anillos de seis miembros compuestos de boro de 3 coordenadas alternas y oxígeno de 2 coordenadas. Debido a la dificultad de construir modelos desordenados con la densidad correcta con muchos anillos de boroxol , esta vista fue inicialmente controvertida, pero estos modelos se han construido recientemente y exhiben propiedades que coinciden excelentemente con los experimentos. Ahora se reconoce, a partir de estudios experimentales y teóricos, que la fracción de átomos de boro que pertenece a anillos boroxol en B vidrioso 2 O 3 es en algún lugar entre 0,73 y 0,83, con 0,75 ( 3 / 4 ) que corresponde a una relación 1: 1 entre unidades de anillo y sin anillo. El número de anillos de boroxol decae en estado líquido al aumentar la temperatura.
La forma cristalina (α-B 2 O 3 ) (ver estructura en el cuadro de información) se compone exclusivamente de triángulos BO 3 . Esta red trigonal, similar al cuarzo , sufre una transformación similar a un coesita en β-B 2 O 3 monoclínico a varios gigapascales (9.5 GPa).
Preparación
El trióxido de boro se produce tratando bórax con ácido sulfúrico en un horno de fusión . A temperaturas superiores a 750 ° C, la capa de óxido de boro fundido se separa del sulfato de sodio . Luego se decanta, se enfría y se obtiene con una pureza del 96–97%.
Otro método es calentar ácido bórico por encima de ~ 300 ° C. El ácido bórico se descompondrá inicialmente en vapor, (H 2 O (g) ) y ácido metabórico (HBO 2 ) a unos 170 ° C, y un calentamiento adicional por encima de los 300 ° C producirá más vapor y trióxido de diboro. Las reacciones son:
- H 3 BO 3 → HBO 2 + H 2 O
- 2 HBO 2 → B 2 O 3 + H 2 O
El ácido bórico se convierte en B 2 O 3 microcristalino anhidro en un lecho fluidizado calentado. La velocidad de calentamiento cuidadosamente controlada evita el engomado a medida que evoluciona el agua. El óxido de boro fundido ataca a los silicatos. Los tubos grafitizados internamente mediante descomposición térmica de acetileno se pasivan.
La cristalización de α-B 2 O 3 fundido a presión ambiente está fuertemente desfavorecida cinéticamente (compare las densidades de líquido y cristal). Las condiciones de umbral para la cristalización del sólido amorfo son 10 kbar y ~ 200 ° C. Su estructura cristalina propuesta en los grupos espaciales enantiomórficos P3 1 (# 144); P3 2 (# 145) (por ejemplo, γ-glicina) se ha revisado a grupos espaciales enantiomórficos P3 1 21 (# 152); P3 2 21 (# 154) (por ejemplo, α-cuarzo).
El óxido de boro también se formará cuando el diborano (B 2 H 6 ) reaccione con el oxígeno del aire o con trazas de humedad:
- 2B 2 H 6 (g) + 3O 2 (g) → 2B 2 O 3 (s) + 6H 2 (g)
- B 2 H 6 (g) + 3H 2 O (g) → B 2 O 3 (s) + 6H 2 (g)
Aplicaciones
- Agente fundente para vidrio y esmaltes
- Material de partida para la síntesis de otro boro compuestos tales como carburo de boro
- Un aditivo utilizado en fibras de vidrio ( fibras ópticas )
- Componente utilizado en la producción de vidrio de borosilicato.
- La capa de recubrimiento inerte en el proceso de encapsulación líquida de Czochralski para la producción de monocristales de arseniuro de galio
- Como catalizador ácido en síntesis orgánica

