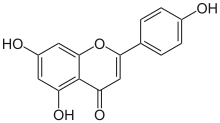
Apigenina - Apigenin
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
4 ', 5,7-trihidroxiflavona
|
|
|
Nombre IUPAC preferido
5,7-Dihidroxi-2- (4-hidroxifenil) -4 H -1-benzopiran-4-ona |
|
| Otros nombres
Apigenina; Manzanilla; Apigenol; Espigenina; Versulina; CI Amarillo natural 1
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Tarjeta de información ECHA |
100.007.540 |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 15 H 10 O 5 | |
| Masa molar | 270,240 g · mol −1 |
| Apariencia | Sólido cristalino amarillo |
| Punto de fusion | 345 a 350 ° C (653 a 662 ° F; 618 a 623 K) |
| UV-vis (λ máx. ) | 267, 296sh, 336 nm en metanol |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
La apigenina (4 ', 5,7-trihidroxiflavona), que se encuentra en muchas plantas, es un producto natural que pertenece a la clase de las flavonas y es la aglicona de varios glucósidos naturales . Es un sólido cristalino amarillo que se ha utilizado para teñir lana.
Fuentes en la naturaleza
La apigenina se encuentra en muchas frutas y verduras, pero el perejil , el apio , el apio nabo y el té de manzanilla son las fuentes más comunes. La apigenina es particularmente abundante en las flores de las plantas de manzanilla y constituye el 68% del total de flavonoides . El perejil seco puede contener alrededor de 45 mg / gramo y la flor de manzanilla seca alrededor de 3-5 mg / gramo de apigenina. El contenido de apigenina del perejil fresco es de 215,5 mg / 100 gramos, que es mucho más alto que la siguiente fuente de alimento más alta, los corazones de apio verde que proporcionan 19,1 mg / 100 gramos.
Biosíntesis
La apigenina se deriva biosintéticamente de la vía general fenilpropanoide y la vía de síntesis de flavonas. La vía fenilpropanoide comienza a partir de los aminoácidos aromáticos L-fenilalanina o L-tirosina, ambos productos de la vía Shikimate . Cuando se parte de L-fenilalanina, primero el aminoácido se desamina de forma no oxidativa por la fenilalanina amoniaco liasa (PAL) para producir cinamato, seguido de oxidación en la posición para por cinamato 4-hidroxilasa (C4H) para producir p- cumarato. Como la L-tirosina ya está oxidada en la posición para , omite esta oxidación y simplemente es desaminada por la tirosina amoniaco liasa (TAL) para llegar al p- cumarato. Para completar la vía general del fenilpropanoide, la ligasa 4-cumarato CoA (4CL) sustituye a la coenzima A (CoA) en el grupo carboxi del p- cumarato. Al entrar en la vía de síntesis de flavonas, la enzima policétido sintasa de tipo III calcona sintasa (CHS) utiliza condensaciones consecutivas de tres equivalentes de malonil CoA seguidas de aromatización para convertir p -cumaroil-CoA en calcona. La calcona isomerasa (CHI) luego isomeriza el producto para cerrar el anillo de pirona para producir naringenina. Finalmente, una enzima flavanona sintasa (FNS) oxida la naringenina a apigenina. Se han descrito previamente dos tipos de FNS; FNS I, una enzima soluble que utiliza 2-oxogluturato, Fe 2+ y ascorbato como cofactores y FNS II, una monooxigenasa de citocromo p450 dependiente de NADPH unida a la membrana.
Glucósidos
Los glucósidos naturales formados por la combinación de apigenina con azúcares incluyen:
- Apiin (apigenin 7- O -apioglucósido), aislado de perejil y apio
- Apigetrina (apigenina 7-glucósido), que se encuentra en el café de diente de león
- Vitexina (apigenina 8- C -glucósido)
- Isovitexina (apigenina 6- C -glucósido)
- Rhoifolina (apigenina 7- O - neohesperidosida )
- Schaftoside (apigenina 6- C -glucósido 8- C -arabinósido)

