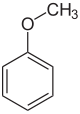
Anisol - Anisole
|
|
|||

|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC
Metoxibenceno
|
|||
|
Nombre IUPAC preferido
Anisol |
|||
| Otros nombres
Metil fenil éter
Fenoximetano |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 506892 | |||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.002.615 |
||
| Número CE | |||
| 2964 | |||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| un numero | 2222 | ||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 7 H 8 O | |||
| Masa molar | 108.140 g · mol −1 | ||
| Apariencia | Líquido incoloro | ||
| Densidad | 0,995 g / cm 3 | ||
| Punto de fusion | -37 ° C (-35 ° F; 236 K) | ||
| Punto de ebullición | 154 ° C (309 ° F; 427 K) | ||
| Solubilidad | Insoluble | ||
| -72,79 · 10 −6 cm 3 / mol | |||
| Riesgos | |||
| Pictogramas GHS |
 
|
||
| Palabra de señal GHS | Advertencia | ||
| H226 , H315 , H319 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P264 , P280 , P302 + 352 , P303 + 361 + 353 , P305 + 351 + 338 , P321 , P332 + 313 , P337 + 313 , P362 , P370 + 378 , P403 + 235 , P501 | |||
| NFPA 704 (diamante de fuego) | |||
| Dosis o concentración letal (LD, LC): | |||
|
LD 50 ( dosis media )
|
3700 mg / kg (rata, oral) | ||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El anisol , o metoxibenceno , es un compuesto orgánico con la fórmula CH 3 OC 6 H 5 . Es un líquido incoloro con olor que recuerda a semilla de anís , y de hecho muchos de sus derivados se encuentran en fragancias naturales y artificiales. El compuesto se fabrica principalmente de forma sintética y es un precursor de otros compuestos sintéticos. Es un éter . El anisol es un reactivo estándar de valor práctico y pedagógico.
Puede prepararse mediante la síntesis de éter de Williamson ; se hace reaccionar fenóxido de sodio con un haluro de metilo para producir anisol.
Reactividad
El anisol sufre una reacción de sustitución aromática electrofílica a una velocidad más rápida que el benceno , que a su vez reacciona más rápidamente que el nitrobenceno . El grupo metoxi es un grupo que dirige orto / para , lo que significa que la sustitución electrofílica ocurre preferentemente en estos tres sitios. La nucleofilia mejorada del anisol frente al benceno refleja la influencia del grupo metoxi , que hace que el anillo sea más rico en electrones. El grupo metoxi afecta fuertemente a la nube pi del anillo como donador de electrones mesomérico , más que como grupo inductivo sustractor de electrones a pesar de la electronegatividad del oxígeno . Expresado de forma más cuantitativa, la constante de Hammett para la para-sustitución del anisol es -0,27.
Ilustrativo de su nucleofilia , el anisol reacciona con anhídrido acético para dar 4-metoxiacetofenona :
- CH 3 OC 6 H 5 + (CH 3 CO) 2 O → CH 3 OC 6 H 4 C (O) CH 3 + CH 3 CO 2 H
A diferencia de la mayoría de las acetofenonas, pero reflejando la influencia del grupo metoxi, la metoxiacetofenona sufre una segunda acetilación . Se han demostrado muchas reacciones relacionadas. Por ejemplo, P 4 S 10 convierte el anisol en el reactivo de Lawesson , [(CH 3 OC 6 H 4 ) PS 2 ] 2 .
También indica un anillo rico en electrones, anisol fácilmente formas pi-complejos con carbonilos metálicos , por ejemplo, Cr (η 6 anisol) (CO) 3 .
El enlace éter es muy estable, pero el grupo metilo se puede eliminar con ácido yodhídrico :
- CH 3 OC 6 H 5 + HI → HOC 6 H 5 + CH 3 I
La reducción de abedul de anisol da 1-metoxiciclohexa-1,4-dieno.
Preparación
El anisol se prepara por metilación de fenóxido de sodio con dimetilsulfato o cloruro de metilo:
- 2 C 6 H 5 O - Na + + (CH 3 O) 2 SO 2 → 2 C 6 H 5 OCH 3 + Na 2 SO 4
Aplicaciones
El anisol es un precursor de los perfumes , las feromonas de insectos y los productos farmacéuticos . Por ejemplo, el anetol sintético se prepara a partir de anisol.
La seguridad
Anisol es relativamente no tóxico con un LD 50 de 3.700 mg / kg en ratas. Su principal peligro es su inflamabilidad.
Ver también
- Anethole
- Bromoanisol
- Hidroxianisol butilado
- Éter
- Etil fenil éter
- Fenol
- 2,4,6-tricloroanisol (olor a corcho)
Referencias
-
^ a b c
Nomenclatura de la química orgánica: Recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: La Real Sociedad de Química . 2014. págs. 702–703. doi : 10.1039 / 9781849733069-00648 . ISBN 978-0-85404-182-4.
El anisol, C 6 H 5 -O-CH 3 , es el único nombre de la clase de éteres que se conserva tanto como nombre preferido de la IUPAC como para su uso en la nomenclatura general. Para los nombres IUPAC preferidos, no se permite la sustitución; para la nomenclatura general, se permite la sustitución en el anillo y en la cadena lateral bajo ciertas condiciones (ver P-34.1.1.4).
- ^ Smith, Michael B .; March, Jerry (2007), Química orgánica avanzada: reacciones, mecanismos y estructura (6a ed.), Nueva York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Thomsen, K. Clausen, S. Scheibye, S.-O. Lawesson (1984). "Tiación con 2,4-bis (4-metoxifenil) -1,3,2,4-2,4-disulfuro de ditiadifosfetano: N-metiltiopirrolidona". Síntesis orgánicas . 62 : 158. doi : 10.15227 / orgsyn.062.0158 .CS1 maint: varios nombres: lista de autores ( enlace )
- ^ E. Peter Kündig (2004). "Síntesis de complejos de metales de transición η 6 -Arene". Temas Organomet Chem . 7 : 3-20. doi : 10.1007 / b94489 .
- ^ AJ Birch y KB Chamberlain (1977). "Tricarbonil [(2,3,4,5-η) -2,4-ciclohexadien-1-ona] Hierro y tricarbonil [(1,2,3,4,5-η) -2-Metoxi-2,4 -Ciclohexadien-1-il] Hierro (1+) Hexafluorofosfato (1−) de Anisol ". Síntesis orgánicas . 57 : 107. doi : 10.15227 / orgsyn.057.0107 .
- ^ GS Hiers y FD Hager (1929). "Anisol". Síntesis orgánicas . 9 : 12. doi : 10.15227 / orgsyn.009.0012 .
- ^ a b Helmut Fiege, Heinz-Werner Voges, Toshikazu Hamamoto, Sumio Umemura, Tadao Iwata, Hisaya Miki, Yasuhiro Fujita, Hans-Josef Buysch, Dorothea Garbe, Wilfried Paulus "Derivados del fenol" en la Enciclopedia de química industrial de Ullmann, 2002, Wiley -VCH, Weinheim. doi : 10.1002 / 14356007.a19_313
- ^ a b MSDS Archivado el 1 de julio de 2010 en Wayback Machine.
enlaces externos
- Tarjeta internacional de seguridad química 1014
- Entrada de base de datos de feromonas pherobase