Versicano - Versican
Versican es un proteoglicano de matriz extracelular grande que está presente en una variedad de tejidos humanos. Está codificado por el gen VCAN .
Versican es un proteoglicano de condroitín sulfato grande con una masa molecular aparente de más de 1000 kDa. En 1989, Zimmermann y Ruoslahti clonaron y secuenciaron la proteína central del proteoglicano sulfato de condroitina de fibroblasto. Lo designaron versican en reconocimiento a su estructura modular versátil.
Versican pertenece a la familia de las proteínas lecticanas , con agrecano (abundante en el cartílago ), brevicano y neurocano (proteoglicanos del sistema nervioso) como otros miembros. Versican también se conoce como proteína central de condroitín sulfato proteoglicano 2 o condroitín sulfato proteoglicano 2 (CSPG2) y PG-M.
Estructura
Estos proteoglicanos comparten regiones de unión globulares N-terminal , C-terminal y glicosaminoglicanos (GAG) homólogas .
El dominio globular N-terminal (G1) consta de un bucle similar a Ig y dos módulos de enlace, y tiene propiedades de unión a hialuronano (HA).
Versican se presenta en 5 isoformas: V0, V1, V2, V3, V4. El dominio central de versican V0 contiene los dominios GAG-α y GAG-β. Las isoformas V1 tienen el dominio GAG-β, V2 tiene el dominio GAG-α, V3 carece de dominios de unión a GAG y V4 tiene una parte del dominio GAG-β. Los GAG, que se componen de unidades de disacáridos repetidos, contribuyen a la carga negativa y muchas otras propiedades de los proteoglicanos.
El dominio globular C-terminal (G3) consta de una o dos repeticiones del factor de crecimiento epidérmico (EGF), un dominio de lectina de tipo C y un dominio similar a la proteína reguladora del complemento (CRP). El dominio C-terminal se une a una variedad de ligandos en ECM que contribuyen significativamente a las funciones de los lecticans.
Función
Se ha estudiado ampliamente el papel del versicano en la adhesión, migración y proliferación celular . Versican a menudo se considera una molécula anti-adherencia. Teniendo en cuenta el gran tamaño (> 1000 kDa) y la capacidad de hidratación del versican, es posible que la interacción de las integrinas (gran familia de moléculas de adhesión celular) con sus receptores de superficie celular se vea obstaculizada estéricamente.
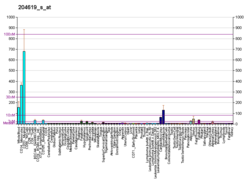
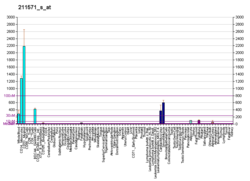
La expresión del versicano se observa en varios tejidos adultos, como los vasos sanguíneos, la piel y el corazón en desarrollo. Las células del músculo liso de los vasos sanguíneos, las células epiteliales de la piel y las células del sistema nervioso central y periférico son algunos ejemplos de tipos de células que se expresan fisiológicamente versican. Versican está involucrado en el desarrollo, guiando la migración de células embrionarias importante en la formación del corazón y delineando el camino para la migración de células de la cresta neural.
N-terminal
El N-terminal de versican tiene un papel importante en el mantenimiento de la integridad del ECM al interactuar con hialuronano. También se han estudiado sus interacciones con la proteína de enlace.
Región de unión de glucosaminoglicanos
El dominio central de Versican está decorado con glicosaminoglicanos. La diversidad estructural y funcional de Versican aumenta por las variaciones en los patrones de sulfatación de GAG y el tipo de cadenas de GAG unidas a la proteína central. Hay un solo gen versicano, sin embargo, el corte y empalme alternativo de su ARNm produce 4 isoformas versican distintas que difieren en su número potencial de cadenas GAG. Todas las isoformas tienen dominios homólogos N-terminal (unión a HA) y C-terminal (tipo lectina). El dominio central del versicano V0 contiene los dominios GAG-α y GAG-β. Las isoformas V1 tienen el dominio GAG-β, V2 tiene el dominio GAG-α y V3 carece de cualquier dominio de unión GAG y solo consta de los dominios globulares N-terminal y C-terminal. Se sabe que las isoformas se expresan diferencialmente en diferentes tipos de tejidos. Aún no se ha determinado la importancia biológica del empalme alternativo.
Debido a sus grupos carboxilo o sulfatos cargados negativamente, las cadenas de sulfato de condroitina son atraídas por varias moléculas cargadas positivamente, como ciertos factores de crecimiento, citocinas y quimiocinas. Esta interacción en la matriz extracelular o en la superficie celular es importante en la formación de gradientes inmovilizados de estos factores, su protección frente a la escisión proteolítica y su presentación a receptores específicos de la superficie celular. La unión del versicano con las moléculas de adhesión de leucocitos L-selectina, P-selectina y CD44 también está mediada por la interacción de las cadenas CS del versicano con el dominio de unión a carbohidratos de estas moléculas. Tanto CD44 como L-selectina se han implicado en el tráfico de leucocitos. También se ha examinado la capacidad del versicano para unirse a un gran panel de quimiocinas y las consecuencias biológicas de dicha unión. Versican puede unirse a quimiocinas específicas a través de sus cadenas CS y esta interacción regula negativamente la función de las quimiocinas. Recientemente, a la luz de los resultados de que las isoformas V1 y V2 de versican tienen efectos opuestos sobre la proliferación celular, el dominio de glicosaminoglicano GAG-β se ha implicado en la proliferación celular potenciada por versican y la reducción de la apoptosis celular inducida por versican.
C-terminal
El C-terminal de Versican interactúa con una variedad de moléculas en la matriz. Una familia importante de ligandos es la familia de la tenascina . Por ejemplo, el dominio C-lectina del versicano interactúa con tenascina R a través de su dominio de repetición 3-5 de fibronectina tipo III (FnIII) de una manera dependiente del calcio, in vivo . Los diferentes dominios de tenascina interactúan con una amplia gama de receptores celulares, incluidas las integrinas, las moléculas de adhesión celular y los miembros de las familias de proteoglicanos sindecano y glipicano. El dominio C-terminal de Versican interactúa con la fibulina-2 , una proteína cuya expresión está asociada con la del versican en el corazón en desarrollo. El dominio EGF del C-terminal de versican también se une a la molécula receptora de EGF in vivo .
Significación clínica
Versican es un factor clave en la inflamación a través de interacciones con moléculas de adhesión en las superficies de leucocitos inflamatorios e interacciones con quimiocinas que participan en el reclutamiento de células inflamatorias.
En el sistema nervioso central adulto, el versicano se encuentra en las redes perineuronales , donde puede estabilizar las conexiones sinápticas. Versican también puede inhibir la regeneración del sistema nervioso y el crecimiento axonal después de una lesión en el sistema nervioso central.
Cáncer y metástasis
El aumento de la expresión de versicano se observa a menudo en el crecimiento de tumores en tejidos como mama, cerebro, ovario, tracto gastrointestinal, próstata y melanoma , sarcoma y mesotelioma peritoneal . Una quinta isoforma de versicano, V4, que es similar a V1 pero con una región beta-GAG acortada, está presente y aumentada en el cáncer de mama humano .
Versican es necesario para que el carcinoma de pulmón de Lewis en ratones metastatice a pulmón, hígado y glándulas suprarrenales, actuando a través de TLR2 para activar las células mieloides y producir TNF-alfa .
Trastornos pulmonares
Versican aumenta en la matriz extracelular tisular cambiante en los trastornos pulmonares inflamatorios como la enfermedad pulmonar obstructiva crónica (EPOC), el asma y el síndrome de bronquiolitis obliterante (BOS). Las células ( miofibroblastos , macrófagos y otras células inflamatorias) pueden migrar más fácilmente a través de la matriz extracelular que tiene un mayor contenido de versican.
Trastornos de la piel
Los depósitos de versican no están presentes en la piel normal, pero se encuentran en la dermis reticular durante la formación de cicatrices queloides , una afección en la que la formación de cicatrices se descontrola y se produce un crecimiento excesivo de tejido cutáneo en el lugar de la herida .
Interacciones
Se ha demostrado que Versican interactúa con hialuronano y una proteína de enlace (proteína 1 de enlace de hialuronano y proteoglicano; HAPLN1 ).
Referencias
Otras lecturas
- Wight TN, Merrilees MJ (2004). "Proteoglicanos en aterosclerosis y reestenosis: roles clave para versican" . Circ. Res . 94 (9): 1158–67. doi : 10.1161 / 01.RES.0000126921.29919.51 . PMID 15142969 .
- Kenagy RD, Plaas AH, Wight TN (2006). "Degradación Versican y enfermedad vascular" . Tendencias Cardiovasc. Med . 16 (6): 209–15. doi : 10.1016 / j.tcm.2006.03.011 . PMC 3169384 . PMID 16839865 .
- Perides G, Rahemtulla F, Lane WS, Asher RA, Bignami A (1992). "Aislamiento de un proteoglicano de agregación grande del cerebro humano" . J. Biol. Chem . 267 (33): 23883–7. doi : 10.1016 / S0021-9258 (18) 35919-2 . PMID 1429726 .
- Iozzo RV, Naso MF, Cannizzaro LA, Wasmuth JJ, McPherson JD (1993). "Mapeo del gen del proteoglicano versicano (CSPG2) al brazo largo del cromosoma humano 5 (5q12-5q14)". Genómica . 14 (4): 845–51. doi : 10.1016 / S0888-7543 (05) 80103-X . PMID 1478664 .
- Perides G, Lane WS, Andrews D, Dahl D, Bignami A (1989). "Aislamiento y caracterización parcial de una proteína de unión a hialuronato glial" . J. Biol. Chem . 264 (10): 5981–7. doi : 10.1016 / S0021-9258 (18) 83646-8 . PMID 2466833 .
- Bignami A, Lane WS, Andrews D, Dahl D (1989). "Similitud estructural de proteínas de unión de hialuronato en cerebro y cartílago". Brain Res. Bull . 22 (1): 67–70. doi : 10.1016 / 0361-9230 (89) 90129-9 . PMID 2469524 . S2CID 25745740 .
- Zimmermann DR, Ruoslahti E (1990). "Múltiples dominios del proteoglicano de fibroblastos grandes, versican" . EMBO J . 8 (10): 2975–81. doi : 10.1002 / j.1460-2075.1989.tb08447.x . PMC 401368 . PMID 2583089 .
- Krusius T, Gehlsen KR, Ruoslahti E (1987). "Una proteína de núcleo de proteoglicano de sulfato de condroitina de fibroblasto contiene secuencias similares a lectinas y similares a factores de crecimiento" . J. Biol. Chem . 262 (27): 13120–5. doi : 10.1016 / S0021-9258 (18) 45176-9 . PMID 2820964 .
- Naso MF, Zimmermann DR, Iozzo RV (1995). "Caracterización de la estructura genómica completa del gen versicano humano y análisis funcional de su promotor" . J. Biol. Chem . 269 (52): 32999–3008. doi : 10.1016 / S0021-9258 (20) 30090-9 . PMID 7528742 .
- Brown DM, Graemiger RA, Hergersberg M, Schinzel A, Messmer EP, Niemeyer G, Schneeberger SA, Streb LM, Taylor CM, Kimura AE (1995). "Vínculo genético de la enfermedad de Wagner y vitreorretinopatía erosiva al cromosoma 5q13-14". Arco. Oftalmol . 113 (5): 671–5. doi : 10.1001 / archopht.1995.01100050139045 . PMID 7748141 .
- Dours-Zimmermann MT, Zimmermann DR (1995). "Un nuevo dominio de unión de glucosaminoglicanos identificado en dos variantes de empalme alternativas de versican humano" . J. Biol. Chem . 269 (52): 32992–8. doi : 10.1016 / S0021-9258 (20) 30089-2 . PMID 7806529 .
- Zako M, Shinomura T, Ujita M, Ito K, Kimata K (1995). "Expresión de PG-M (V3), una forma de empalme alternativo de PG-M sin una unión de sulfato de condroitina en la región en tejidos humanos y de ratón" . J. Biol. Chem . 270 (8): 3914–8. doi : 10.1074 / jbc.270.8.3914 . PMID 7876137 . S2CID 26136117 .
- Yao LY, Moody C, Schönherr E, Wight TN, Sandell LJ (1994). "Identificación del proteoglicano versicano en células de músculo liso y aorta mediante análisis de secuencia de ADN, hibridación in situ e inmunohistoquímica". Matrix Biol . 14 (3): 213-25. doi : 10.1016 / 0945-053X (94) 90185-6 . PMID 7921538 .
- Bode-Lesniewska B, Dours-Zimmermann MT, Odermatt BF, Briner J, Heitz PU, Zimmermann DR (1996). "Distribución del versican proteoglicano de agregación grande en tejidos humanos adultos" . J. Histochem. Cytochem . 44 (4): 303–12. doi : 10.1177 / 44.4.8601689 . PMID 8601689 . S2CID 23190687 .
- Sartipy P, Johansen B, Camejo G, Rosengren B, Bondjers G, Hurt-Camejo E (1996). "Unión de fosfolipasa A2 humana tipo II a proteoglicanos. Efecto diferencial de los glicosaminoglicanos sobre la actividad enzimática" . J. Biol. Chem . 271 (42): 26307–14. doi : 10.1074 / jbc.271.42.26307 . PMID 8824283 . S2CID 21537718 .
- Sartipy P, Bondjers G, Hurt-Camejo E (1999). "La fosfolipasa A2 tipo II se une a la matriz extracelular de biglicano: modulación de su actividad sobre LDL por colocalización en matrices de glicosaminoglicanos" . Arterioscler. Trombo. Vasc. Biol . 18 (12): 1934–41. doi : 10.1161 / 01.ATV.18.12.1934 . PMID 9848887 .
- Perveen R, Hart-Holden N, Dixon MJ, Wiszniewski W, Fryer AE, Brunner HG, Pinkners AJ, van Beersum SE, Black GC (1999). "Localización genética y física refinada del locus de la enfermedad de Wagner (WGN1) y los genes CRTL1 y CSPG2 en una región de 2 a 2,5 cM del cromosoma 5q14.3" . Genómica . 57 (2): 219-26. doi : 10.1006 / geno.1999.5766 . PMID 10198161 . S2CID 43814139 .
- Lemire JM, Braun KR, Maurel P, Kaplan ED, Schwartz SM, Wight TN (1999). "Isoformas de Versican / PG-M en células de músculo liso vascular" . Arterioscler. Trombo. Vasc. Biol . 19 (7): 1630–9. doi : 10.1161 / 01.ATV.19.7.1630 . PMID 10397680 .
-
Yan Y, Qin D, Hu B, Zhang C, Liu S, Wu D, Huang W, Huang X, Wang L, Chen X, Zhang L (abril de 2019). "La eliminación de miR-126a promovió la inflamación y el envejecimiento hepático en un modelo de ratón de colestasis" . Terapia Molecular-Ácidos Nucleicos . 16 : 494–504. doi : 10.1016 / j.omtn.2019.04.002 . PMC 6495079 . PMID 31051334 .
Versican identificado como un objetivo directo de miR-126a-5p que induce el acortamiento de los telómeros, la senescencia y el activador de la vía del factor nuclear κB (NF-κB)
enlaces externos
- La entrada de GeneReviews / NCBI / NIH / UW sobre la vitreorretinopatía relacionada con VCAN incluye: degeneración vitreorretiniana de Wagner (síndrome de Wagner), vitreorretinopatía erosiva (ERVR)
- Versicans en los títulos de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .