Yoduro de talio (I) - Thallium(I) iodide
|
|
| Nombres | |
|---|---|
| Otros nombres
Yoduro de talio
yoduro de talio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.029.272 |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| TlI | |
| Masa molar | 331,287 g / mol |
| Apariencia | cristales amarillos |
| Densidad | 7,1 g / cm 3 |
| Punto de fusion | 441,7 ° C (827,1 ° F; 714,8 K) |
| Punto de ebullición | 824 ° C (1,515 ° F; 1,097 K) |
| 0,085 g / L (25 ° C) | |
| Solubilidad | insoluble en alcohol |
| −82,2 · 10 −6 cm 3 / mol | |
| Peligros | |
| Muy tóxico ( T + ) Peligroso para el medio ambiente ( N ) |
|
| Frases R (desactualizadas) | R26 / 28 , R33 , R51 / 53 |
| Frases S (desactualizadas) | (S1 / 2) , S13 , S28 , S45 , S61 |
| punto de inflamabilidad | No es inflamable |
| Compuestos relacionados | |
|
Otros aniones
|
Fluoruro de talio (I) Cloruro de talio (I) Bromuro de talio (I) |
|
Otros cationes
|
Yoduro de galio (I) Yoduro de indio (I) |
|
Compuestos relacionados
|
Yoduro de mercurio (II) Yoduro de plomo (II) |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El yoduro de talio (I) es un compuesto químico con la fórmula TlI . Es inusual por ser uno de los pocos yoduros metálicos insolubles en agua , junto con AgI , CuI , SnI 2 , SnI 4 , PbI 2 y HgI 2 .
Química
TlI puede formarse en solución acuosa por metátesis de cualquier sal soluble de talio con ión yoduro. También se forma como un subproducto en la yodación de fenoles promovida por talio con acetato de talio (I).
Los intentos de oxidar TlI a yoduro de talio (III) fracasan, ya que la oxidación produce el triyoduro de talio (I) , Tl + I 3 - .
Propiedades físicas
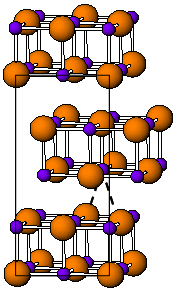
La forma de TlI a temperatura ambiente es amarilla y tiene una estructura ortorrómbica que puede considerarse una estructura de NaCl distorsionada. Se cree que la estructura distorsionada es causada por interacciones favorables talio-talio, la distancia Tl-Tl más cercana es 383 pm. A 175 ° C, la forma amarilla se transforma en una forma roja de CsCl . Esta transición de fase va acompañada de un salto de aproximadamente dos órdenes de magnitud en la conductividad eléctrica. La estructura de CsI se puede estabilizar a temperatura ambiente dopando TlI con otros haluros como RbI, CsI, KI, AgI, TlBr y TlCl. Por tanto, la presencia de impurezas podría ser responsable de la coexistencia de las fases TlI cúbica y ortorrómbica en condiciones ambientales. A alta presión, 160 kbar, TlI se convierte en un conductor metálico. Las películas de TlI delgadas en nanómetros que crecen sobre sustratos de LiF, NaCl o KBr exhiben la estructura cúbica de sal de roca .
Aplicaciones
Se añade yoduro de talio (I) a las lámparas de arco de mercurio para mejorar su rendimiento. La luz producida se encuentra principalmente en la parte azul verdosa del espectro de luz visible menos absorbida por el agua, por lo que se han utilizado para iluminación subacuática. El yoduro de talio (I) también se usa en cantidades traza con NaI o CsI para producir centelleadores usados en detectores de radiación.
Ocurrencia natural
El yoduro de talio (I) natural se descubrió recientemente, como un polimorfo ortorrómbico llamado nataliyamalikita. Es de origen fumarólico.
La seguridad
Como todos los compuestos de talio, el yoduro de talio (I) es muy tóxico.
Referencias
Fuentes citadas
- Haynes, William M., ed. (2011). Manual CRC de Química y Física (92ª ed.). Boca Raton, FL: CRC Press . ISBN 1439855110 .
