Rucaparib - Rucaparib
 | |
| Datos clinicos | |
|---|---|
| Pronunciación | / R U k æ p ər ɪ b / Roo- KAP -ər-ib |
| Nombres comerciales | Rubraca |
| Otros nombres | AG014699 |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a617002 |
| Datos de licencia | |
Categoría de embarazo |
|
| Vías de administración |
Por vía oral ( tabletas ) |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 30–45% ( T máx = 1,9 horas) |
| Enlace proteico | 70% ( in vitro ) |
| Metabolismo | Hígado (principalmente CYP2D6 ; 1A2 y 3A4 en menor grado) |
| Vida media de eliminación | 17-19 horas |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Ligando PDB | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA |
100.247.490 |
| Datos químicos y físicos | |
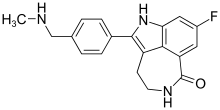
| Fórmula | C 19 H 18 F N 3 O |
| Masa molar | 323,371 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
Rucaparib , vendido bajo la marca Rubraca , es un inhibidor de PARP utilizado como agente anticanceroso. Rucaparib es un fármaco farmacéutico de primera clase dirigido a la enzima reparadora del ADN poli-ADP ribosa polimerasa-1 (PARP-1). Está aprobado en los Estados Unidos y en Europa como tratamiento de tercera línea en el cáncer de ovario con mutación BRCA .
Se puede tomar por vía oral en forma de tabletas.
Los efectos secundarios más comunes incluyen cansancio o debilidad, náuseas (malestar), niveles elevados de creatinina (que pueden indicar problemas renales) y enzimas hepáticas en la sangre (que pueden indicar daño hepático), vómitos, anemia (recuentos bajos de glóbulos rojos). ), disminución del apetito, disgeusia (alteraciones del gusto), diarrea, trombocitopenia (niveles bajos de plaquetas) y dolor abdominal (dolor de estómago).
Usos médicos
Rucaparib está indicado como monoterapia para el tratamiento de mantenimiento de adultos con cáncer de ovario epitelial de alto grado, de trompas de Falopio o peritoneal primario recidivante y sensible al platino que responden (total o parcialmente) a la quimioterapia a base de platino.
Rucaparib está indicado como tratamiento en monoterapia de adultos con cáncer de ovario, de trompas de Falopio o primario peritoneal primario, con mutación de BRCA (de línea germinal y / o somático) sensible al platino, en recaída o progresiva, que hayan sido tratados con dos o más líneas anteriores. de quimioterapia a base de platino, y que no pueden tolerar más quimioterapia a base de platino.
Desarrollo
Fue descubierto como parte de una colaboración entre científicos que trabajan en el Instituto Norte de Investigación del Cáncer y la Escuela de Medicina de la Universidad de Newcastle y Agouron Pharmaceuticals en San Diego, California. Está siendo desarrollado por Clovis Oncología .
En diciembre de 2016, la Administración de Drogas y Alimentos de los EE. UU . (FDA) otorgó una aprobación acelerada para su uso en casos de cáncer de ovario avanzado pretratado .
En la Unión Europea fue designado medicamento huérfano el 10 de octubre de 2012. El 22 de marzo de 2018, el Comité de Medicamentos de Uso Humano (CHMP) adoptó un dictamen positivo, recomendando la concesión de una autorización de comercialización condicional, destinada al tratamiento de cáncer de ovario recidivante o progresivo. Fue aprobado para uso médico en la Unión Europea en mayo de 2018.
Farmacología
Mecanismo de acción
Rucaparib inhibe "la contracción del músculo liso vascular aislado, incluida la de los tumores de pacientes con cáncer. También reduce la migración de algunas células cancerosas y normales en cultivo".
Como inhibidor de PARP , se espera que rucaparib sea más eficaz en el 9% de los cánceres de páncreas con una mutación BRCA (BRCA1 o BRCA2).
Ensayos clínicos
Después de la aprobación de la FDA, se iniciaron los estudios de mCRPC TRITON2 y TRITON3 para determinar cómo responderán los pacientes con cáncer de próstata al fármaco rucaparib. Los estudios para estos dos ensayos aún están en curso y las fechas estimadas para los primeros resultados oscilan entre 2019 y 2022.
ARIEL3 y ARIEL4 son dos estudios de fase III aleatorizados, doble ciego. El estudio ARIEL3 se diseñó para evaluar el efecto del agente en investigación como tratamiento de mantenimiento para las pacientes con cáncer de ovario avanzado sensible al platino en comparación con placebo después de su respuesta a al menos dos quimioterapias anteriores. Los resultados de primera línea del estudio se presentaron en el congreso ESMO 2017 y, inmediatamente después, se publicaron en la revista Lancet en septiembre de 2017. Los hallazgos mostraron una mejora significativa en la supervivencia libre de progresión (SLP) en pacientes tratados con Rubraca que placebo. Recientemente, en octubre de 2017, se envió a la FDA una sNDA complementaria para el tratamiento de mantenimiento rucaparib ARIEL3.
El ensayo ARIEL4 aún está en curso para evaluar cómo responderán mejor los pacientes al tratamiento con rucaparib en comparación con la quimioterapia. La fecha estimada de recopilación de datos para la medición del resultado primario será junio de 2022.
Ver también
Referencias
enlaces externos
- "Rucaparib" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- Ensayo clínico número NCT01968213 para "Un estudio de rucaparib como mantenimiento del cambio después de la quimioterapia basada en platino en pacientes con cáncer epitelial de ovario, peritoneal primario o de trompas de Falopio, peritoneal primario o endometrioide sensible al platino de alto grado (ARIEL3)" en ClinicalTrials.gov
