Mentol - Menthol
|
|
|||

|
|||
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
5-metil-2- (propan-2-il) ciclohexan-1-ol |
|||
| Otros nombres
2-Isopropil-5-metilciclohexan-1-ol
2-Isopropil-5-metilciclohexanol 3- p - Metanol Hexahidrotimol Mentomentol Alcanfor de menta |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Tarjeta de información ECHA |
100.016.992 |
||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 10 H 20 O | |||
| Masa molar | 156,269 g · mol −1 | ||
| Apariencia | Sólido cristalino blanco o incoloro | ||
| Densidad | 0,890 g · cm −3 , sólido (racémico o (-) - isómero) |
||
| Punto de fusion | 36–38 ° C (97–100 ° F; 309–311 K) racémico 42–45 ° C, (-) - isómero, forma cristalina α |
||
| Punto de ebullición | 214,6 ° C (418,3 ° F; 487,8 K) | ||
| Isómero (-) ligeramente soluble | |||
| Riesgos | |||
| Principales peligros | Irritante, inflamable | ||
| Ficha de datos de seguridad |
Ver: página de datos Ficha de datos de seguridad externa |
||
| Frases R (desactualizadas) | R37 / 38 , R41 | ||
| Frases S (desactualizadas) | S26 , S36 | ||
| NFPA 704 (diamante de fuego) | |||
| punto de inflamabilidad | 93 ° C (199 ° F; 366 K) | ||
| Compuestos relacionados | |||
|
Alcoholes relacionados
|
Ciclohexanol , pulegol , dihidrocarveol , piperitol |
||
|
Compuestos relacionados
|
Mentona , menteno , timol , p - cimeno , citronelal |
||
| Página de datos complementarios | |||
|
Índice de refracción ( n ), constante dieléctrica (ε r ), etc. |
|||
|
Datos termodinámicos |
Comportamiento de fase sólido-líquido-gas |
||
| UV , IR , RMN , MS | |||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El mentol es un compuesto orgánico elaborado sintéticamente u obtenido de los aceites de menta de maíz , menta piperita u otras mentas . Es una sustancia cerosa, cristalina , transparente o de color blanco, que es sólida a temperatura ambiente y se funde ligeramente por encima.
La forma principal de mentol que se encuentra en la naturaleza es el (-) - mentol , al que se le asigna la configuración (1 R , 2 S , 5 R ) . El mentol tiene cualidades anestésicas locales y contrairritantes , y se usa ampliamente para aliviar la irritación leve de la garganta . El mentol también actúa como un agonista débil del receptor de opioides κ .
En 2017, fue el medicamento 193 más recetado en los Estados Unidos, con más de dos millones de recetas.
Estructura
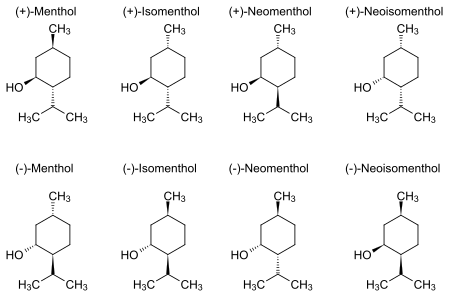
El mentol natural existe como un estereoisómero puro , casi siempre en la forma (1 R , 2 S , 5 R ) (esquina inferior izquierda del diagrama a continuación). Los ocho estereoisómeros posibles son:
En el compuesto natural, el grupo isopropilo está en orientación trans con respecto a los grupos metilo e hidroxilo . Por lo tanto, se puede dibujar de cualquiera de las formas que se muestran:
Los enantiómeros (+) - y (-) - del mentol son los más estables entre estos en función de sus conformaciones de ciclohexano . Con el anillo en sí en una conformación de silla, los tres grupos voluminosos pueden orientarse en posiciones ecuatoriales.
Las dos formas cristalinas del mentol racémico tienen puntos de fusión de 28 ° C y 38 ° C. El (-) - mentol puro tiene cuatro formas cristalinas, de las cuales la más estable es la forma α, las conocidas agujas anchas.
Propiedades biologicas

La capacidad del mentol para activar químicamente los receptores TRPM8 sensibles al frío en la piel es responsable de la conocida sensación de enfriamiento que provoca cuando se inhala, se come o se aplica sobre la piel. En este sentido, es similar a la capsaicina , el químico responsable del picante de los chiles picantes (que estimula los sensores de calor , también sin provocar un cambio real de temperatura).
Las propiedades analgésicas del mentol están mediadas por una activación selectiva de los receptores opioides κ . El mentol bloquea los canales de calcio y los canales de sodio sensibles al voltaje , lo que reduce la actividad neuronal que puede estimular los músculos.
Algunos estudios muestran que el mentol actúa como modulador alostérico positivo del receptor GABA A y aumenta la transmisión gabaérgica en las neuronas PAG. El mentol también comparte anestésicos propiedades similares a propofol , mediante la modulación de los mismos sitios del GABA A receptor .
El mentol se usa ampliamente en el cuidado dental como agente antibacteriano tópico, eficaz contra varios tipos de estreptococos y lactobacilos .
Ocurrencia
Mentha arvensis (menta silvestre) es la principal especie de menta que se utiliza para hacer cristales de mentol natural y hojuelas de mentol natural. Esta especie se cultiva principalmente en laregión de Uttar Pradesh en India .
El mentol se encuentra naturalmente en el aceite de menta (junto con un poco de mentona , el éster acetato de mentilo y otros compuestos), obtenido de Mentha × piperita (menta). El mentol japonés también contiene un pequeño porcentaje del 1- epímero , neomentol.
Biosíntesis
Se ha investigado la biosíntesis del mentol en Mentha × piperita y se han identificado y caracterizado las enzimas implicadas en él. Comienza con la síntesis del terpeno limoneno , seguida de la hidroxilación y luego varios pasos de reducción e isomerización .
Más específicamente, la biosíntesis de (-) - mentol tiene lugar en las células de la glándula secretora de la planta de menta. La geranil difosfato sintasa (GPPS), primero cataliza la reacción de IPP y DMAPP en geranil difosfato . A continuación, la (-) - limoneno sintasa (LS) cataliza la ciclación del difosfato de geranilo en (-) - limoneno . (-) - Limoneno-3-hidroxilasa (L3OH), usando O 2 y NADPH , luego cataliza la hidroxilación alílica de (-) - limoneno en la posición 3 a (-) - trans-isopiperitenol. (-) - trans- isopiperitenol deshidrogenasa (iPD) oxida aún más el grupo hidroxilo en la posición 3 usando NAD + para producir (-) - isopiperitenona. (-) - La isopiperitenona reductasa (iPR) luego reduce el doble enlace entre los carbonos 1 y 2 usando NADPH para formar (+) - cis -isopulegona. (+) - cis -Isopulegona isomerasa (iPI) luego isomeriza el doble enlace restante para formar (+) - pulegona. (+) - Pulegone reductasa (PR) luego reduce este doble enlace usando NADPH para formar (-) - mentona. (-) - La mentona reductasa (MR) luego reduce el grupo carbonilo usando NADPH para formar (-) - mentol.
Producción
El mentol natural se obtiene congelando aceite de menta . Los cristales de mentol resultantes se separan luego por filtración .
La producción mundial total de mentol en 1998 fue de 12.000 toneladas, de las cuales 2.500 toneladas fueron sintéticas. En 2005, la producción anual de mentol sintético fue casi el doble. Los precios están en el rango de $ 10-20 / kg con picos en la región de $ 40 / kg, pero han llegado hasta $ 100 / kg. En 1985, se estimó que China producía la mayor parte del suministro mundial de mentol natural, aunque parece que India ha empujado a China al segundo lugar.
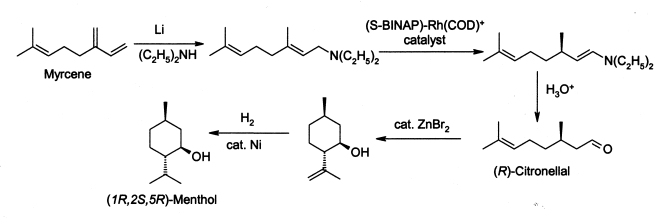
El mentol se fabrica como un enantiómero único (94% ee ) en la escala de 3.000 toneladas por año por Takasago International Corporation . El proceso involucra una síntesis asimétrica desarrollada por un equipo liderado por Ryōji Noyori , quien ganó el Premio Nobel de Química en 2001 en reconocimiento a su trabajo en este proceso:
El proceso comienza formando una amina alílica a partir del mirceno , que sufre una isomerización asimétrica en presencia de un complejo de rodio BINAP para dar (después de la hidrólisis ) R - citronelal enantioméricamente puro . Este se cicla mediante una reacción de carbonil-eno iniciada por bromuro de zinc para dar isopulegol , que luego se hidrogena para dar mentol (1 R , 2 S , 5 R ) puro.
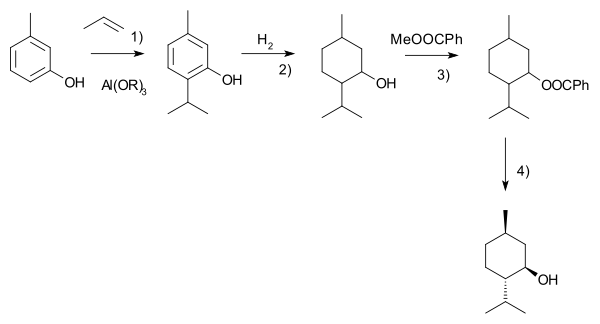
Otro proceso comercial es el proceso Haarmann-Reimer (después de la empresa Haarmann & Reimer, ahora parte de Symrise ). Este proceso parte de m -cresol que se alquila con propeno a timol . Este compuesto se hidrogena en el siguiente paso. El mentol racémico se aísla por destilación fraccionada . Los enantiómeros se separan por resolución quiral en reacción con benzoato de metilo , cristalización selectiva seguida de hidrólisis.
El mentol racémico también se puede formar por hidrogenación de timol , mentona o pulegona . En ambos casos con procesamiento adicional (resolución de arrastre cristalizante del conglomerado de benzoato de mentilo) es posible concentrar el enantiómero L , sin embargo, esto tiende a ser menos eficiente, aunque los costos de procesamiento más altos pueden compensarse con costos de materia prima más bajos. Una ventaja adicional de este proceso es que el D- mentol se vuelve asequible para su uso como auxiliar quiral, junto con el antípodo L más habitual .
Aplicaciones
El mentol se incluye en muchos productos y por diversas razones. Éstos incluyen:
- En productos de venta libre para el alivio a corto plazo del dolor de garganta leve y la irritación leve de la boca o la garganta.
- Ejemplos: bálsamos labiales y medicamentos para la tos .
- Como antipruriginoso para reducir el picor.
- Como analgésico tópico , se utiliza para aliviar dolores y molestias menores, como calambres musculares, esguinces, dolores de cabeza y afecciones similares, solo o combinado con productos químicos como alcanfor , aceite de eucalipto o capsaicina . En Europa, tiende a aparecer como un gel o una crema, mientras que en los EE. UU. Se utilizan con mucha frecuencia los parches y las mangas corporales.
- Ejemplos: Tiger Balm , o IcyHot parches o rodilla / codo mangas .
- Como potenciador de la penetración en la administración transdérmica de fármacos .
- En descongestionantes para el pecho y los senos nasales (crema, parche o inhalador nasal).
- Ejemplos: Vicks VapoRub , Mentholatum , VapoRem, Mentisan.
- En ciertos medicamentos que se utilizan para tratar las quemaduras solares , ya que proporciona una sensación refrescante (entonces a menudo se asocia con el aloe ).
- En productos para después del afeitado para aliviar la irritación causada por el afeitado .
- Como aditivo de tabaco para fumar en algunas marcas de cigarrillos , para dar sabor y para reducir la irritación de la garganta y los senos nasales causada por fumar. El mentol también aumenta la densidad del receptor de nicotina, aumentando el potencial adictivo de los productos de tabaco.
- Se utiliza comúnmente en productos de higiene bucal y remedios para el mal aliento, como enjuagues bucales , pasta de dientes , aerosoles para la boca y la lengua, y más generalmente como agente aromatizante de alimentos; como en la goma de mascar y los caramelos .
- Como plaguicida contra los ácaros traqueales de las abejas melíferas .
- En perfumería , el mentol se usa para preparar ésteres de mentilo para enfatizar notas florales (especialmente rosa).
- En primeros auxilios, productos como "hielo mineral" para producir un efecto refrescante como sustituto del hielo real en ausencia de agua o electricidad (bolsa, parche / manga corporal o crema).
- En varios parches que van desde parches para reducir la fiebre aplicados en la frente de los niños hasta "parches para los pies" para aliviar numerosas dolencias (estas últimas son mucho más frecuentes y elaboradas en Asia , especialmente en Japón : algunas variedades usan "protuberancias funcionales" o pequeñas protuberancias para masajear los pies, además de calmarlos y enfriarlos).
- En algunos productos de belleza, como acondicionadores para el cabello, a base de ingredientes naturales (por ejemplo, St. Ives).
- Como antiespasmódico y relajante del músculo liso en endoscopia digestiva alta .
En química orgánica , el mentol se utiliza como auxiliar quiral en síntesis asimétrica . Por ejemplo, los ésteres de sulfinato hechos a partir de cloruros de sulfinilo y mentol se pueden usar para preparar sulfóxidos enantioméricamente puros por reacción con reactivos de organolitio o reactivos de Grignard . El mentol reacciona con ácidos carboxílicos quirales para dar ésteres de mentilo diastereómicos, que son útiles para la resolución quiral .
- Se puede utilizar como catalizador para la producción de sodio para el químico aficionado a través del proceso de reducción de magnesio catalizado por alcohol.
- El mentol es potencialmente ergogénico (mejora el rendimiento) para el rendimiento deportivo en entornos calurosos.
Reacciones
El mentol reacciona de muchas formas como un alcohol secundario normal. Se oxida a mentona por agentes oxidantes como el ácido crómico o el dicromato , aunque en algunas condiciones la oxidación puede ir más allá y romper el anillo. El mentol se deshidrata fácilmente para dar principalmente 3-mentano, por la acción del ácido sulfúrico al 2% . El pentacloruro de fósforo (PCl 5 ) da cloruro de mentilo.
Historia
En Occidente , el mentol fue aislado por primera vez en 1771 por el alemán Hieronymus David Gaubius . Las primeras caracterizaciones fueron realizadas por Oppenheim, Beckett, Moriya y Atkinson. Fue nombrado por FL Alphons Oppenheim (1833–1877) en 1861.
Estado compendial
- Farmacopea de los Estados Unidos 23
- Farmacopea japonesa 15
- Códice de productos químicos alimentarios
La seguridad
La dosis letal estimada de mentol (y aceite de menta ) en humanos puede ser tan baja como 50-500 mg / kg, (LD50 aguda: 3300 mg / kg [rata]. 3400 mg / kg [ratón]. 800 mg / kg [ Gato]).
Se ha informado de supervivencia después de dosis de 8 a 9 g. Los efectos de sobredosis son dolor abdominal, ataxia, fibrilación auricular, bradicardia, coma, mareos, letargo, náuseas, erupción cutánea, temblores, vómitos, vértigo.
Ver también
Referencias
Otras lecturas
- Turner, EE; Harris, MM (1952). Química Orgánica . Londres: Longmans, Green & Co.
- Manual de Química y Física (71ª ed.). Ann Arbor, MI: CRC Press. 1990.
- The Merck Index (7ª ed.). Rahway, Nueva Jersey: Merck & Co. 1960.
- "Perfil químico aromático: mentol". Perfumista y saborista . 32 (12): 38–47. Diciembre de 2007.
- Colacot, TJ (1 de abril de 2002). "Premio Nobel de Química 2001: reconocimiento oportuno de reacciones quirales catalizadas por rodio, rutenio y osmio" . Platino Metales Rev . 46 (2): 82–83.
enlaces externos
- "Mentol" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- Conferencia Nobel de Ryoji Noyori (2001)
- Una revisión del mentol de Science Creative Quarterly