MG132 - MG132
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
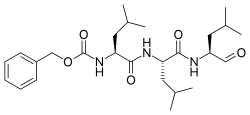
Bencil [(2 S ) -4-metil-1 - {[(2 S ) -4-metil-1 - {[(2 S ) -4-metil-1-oxopentan-2-il] amino} -1- carbamato de oxopentan-2-il] amino} -1-oxopentan-2-il] |
|
| Otros nombres
N- benciloxicarbonilo- L -leucil- L -leucil- L -leucinal
Z-Leu-Leu-Leu-al |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 26 H 41 N 3 O 5 | |
| Masa molar | 475,630 g · mol −1 |
| Apariencia | Blanco sólido |
| Solubilidad | 100 mM en EtOH y DMSO |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
MG132 es un potente, reversible, y permeable a las células inhibidor del proteasoma ( K i = 4 nM). Pertenece a la clase de aldehídos peptídicos sintéticos. Reduce la degradación de proteínas conjugadas con ubiquitina en células de mamíferos y cepas permeables de levadura por el complejo 26S sin afectar sus actividades de ATPasa o isopeptidasa . MG132 activa la quinasa N-terminal c-Jun (JNK1), que inicia la apoptosis . MG132 también inhibe NF-kB activación con un IC 50 de 3 M y previene β-secretasa de escisión.
Mecanismo molecular
Hay varios inhibidores que pueden entrar fácilmente en la célula e inhibir selectivamente la vía de degradación. Incluye aldehídos peptídicos , como Cbz-leu-leu-leucinal (MG132), Cbz-leu-leu- norvalinal ( MG115 ) y acetil-leu-leu-norleucinal ( ALLN ). Estos son análogos de sustrato y potentes inhibidores del estado de transición de la actividad similar a la quimotripsina de la maquinaria del proteasoma . También se sabe que los aldehídos peptídicos inhiben ciertas cisteína proteasas lisosomales y las calpaínas, por lo tanto, MG132 puede no ser un inhibidor exclusivo de la ruta proteasómica.
