Repetición rica en leucina - Leucine-rich repeat
 Un ejemplo de una proteína repetida rica en leucina, un inhibidor de la ribonucleasa porcina
| |||||||||
| Identificadores | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Símbolo | LRR_1 | ||||||||
| Pfam | PF00560 | ||||||||
| Clan pfam | CL0022 | ||||||||
| InterPro | IPR001611 | ||||||||
| SCOP2 | 2bnh / SCOPe / SUPFAM | ||||||||
| Membranome | 605 | ||||||||
| |||||||||
| Variante de repetición rica en leucina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 una variante de repetición rica en leucina con un nuevo motivo estructural de proteína repetitiva
| |||||||||
| Identificadores | |||||||||
| Símbolo | LRV | ||||||||
| Pfam | PF01816 | ||||||||
| Clan pfam | CL0020 | ||||||||
| InterPro | IPR004830 | ||||||||
| SCOP2 | 1lrv / SCOPe / SUPFAM | ||||||||
| Membranome | 737 | ||||||||
| |||||||||
| LRR adyacente | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 internalina h: estructura cristalina de dominios n-terminales fusionados.
| |||||||||
| Identificadores | |||||||||
| Símbolo | LRR_adyacente | ||||||||
| Pfam | PF08191 | ||||||||
| InterPro | IPR012569 | ||||||||
| Membranome | 341 | ||||||||
| |||||||||
| Dominio N-terminal repetido rico en leucina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 decorina dimérica extraída de tejido bovino, forma cristalina 2
| |||||||||
| Identificadores | |||||||||
| Símbolo | LRRNT | ||||||||
| Pfam | PF01462 | ||||||||
| InterPro | IPR000372 | ||||||||
| INTELIGENTE | LRRNT | ||||||||
| SCOP2 | 1m10 / SCOPe / SUPFAM | ||||||||
| Membranome | 127 | ||||||||
| |||||||||
| Dominio N-terminal repetido rico en leucina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
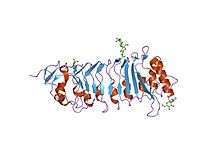 la estructura cristalina de pgip (proteína inhibidora de poligalacturonasa), una proteína repetida rica en leucina involucrada en la defensa de las plantas
| |||||||||
| Identificadores | |||||||||
| Símbolo | LRRNT_2 | ||||||||
| Pfam | PF08263 | ||||||||
| InterPro | IPR013210 | ||||||||
| INTELIGENTE | LRRNT | ||||||||
| SCOP2 | 1m10 / SCOPe / SUPFAM | ||||||||
| |||||||||
| Dominio C-terminal repetido rico en leucina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 tercer dominio lrr de la hendidura de Drosophila
| |||||||||
| Identificadores | |||||||||
| Símbolo | LRRCT | ||||||||
| Pfam | PF01463 | ||||||||
| InterPro | IPR000483 | ||||||||
| INTELIGENTE | LRRCT | ||||||||
| SCOP2 | 1m10 / SCOPe / SUPFAM | ||||||||
| |||||||||
| Clúster de proteína LRV FeS4 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 una variante de repetición rica en leucina con un nuevo motivo estructural de proteína repetitiva
| |||||||||
| Identificadores | |||||||||
| Símbolo | LRV_FeS | ||||||||
| Pfam | PF05484 | ||||||||
| Clan pfam | CL0020 | ||||||||
| InterPro | IPR008665 | ||||||||
| SCOP2 | 1lrv / SCOPe / SUPFAM | ||||||||
| |||||||||
Una repetición rica en leucina (LRR) es un motivo estructural de proteína que forma un pliegue en herradura α / β . Se compone de tramos repetidos de 20-30 aminoácidos que son inusualmente ricos en el aminoácido hidrófobo leucina . Estas repeticiones en tándem comúnmente se pliegan juntas para formar un dominio de proteína de solenoide , denominado dominio de repetición rico en leucina . Por lo general, cada unidad repetida tiene una estructura de hebra beta - giro - hélice alfa , y el dominio ensamblado , compuesto por muchas de estas repeticiones, tiene forma de herradura con una hoja beta paralela interior y una matriz exterior de hélices. Una cara de la hoja beta y un lado de la matriz helicoidal están expuestas al disolvente y, por lo tanto, están dominadas por residuos hidrófilos . La región entre las hélices y las láminas es el núcleo hidrófobo de la proteína y está empaquetada estéricamente con residuos de leucina.
Las repeticiones ricas en leucina con frecuencia participan en la formación de interacciones proteína-proteína.
Ejemplos de
Se han identificado motivos repetidos ricos en leucina en un gran número de proteínas funcionalmente no relacionadas. El ejemplo más conocido es el inhibidor de la ribonucleasa , pero otras proteínas como el regulador de la tropomiosina, la tropomodulina y el receptor tipo toll también comparten el motivo. De hecho, el receptor de tipo toll posee 10 motivos LRR sucesivos que sirven para unir patrones moleculares asociados a patógenos y peligros.
Aunque la proteína LRR canónica contiene aproximadamente una hélice por cada hebra beta, las variantes que forman pliegues de superhélice beta-alfa a veces tienen bucles largos en lugar de hélices que unen sucesivas hebras beta.
Un dominio de variante de repetición rico en leucina (LRV) tiene un nuevo motivo estructural repetitivo que consiste en hélices alfa alternas y 3 10 -helices dispuestas en una superhélice derecha, con la ausencia de las hojas beta presentes en otras repeticiones ricas en leucina.
Dominios asociados
Las repeticiones ricas en leucina a menudo están flanqueadas por dominios ricos en cisteína N-terminal y C-terminal , pero no siempre como es el caso de C5orf36
También co-ocurren con dominios adyacentes LRR. Estos son dominios pequeños, todos de cadena beta , que se han descrito estructuralmente para la proteína Internalina (InlA) y proteínas relacionadas InlB, InlE, InlH de la bacteria patógena Listeria monocytogenes . Su función parece ser principalmente estructural: se fusionan con el extremo C-terminal de las repeticiones ricas en leucina, estabilizando significativamente el LRR y formando una entidad rígida común con el LRR. Ellos mismos no están involucrados en interacciones proteína-proteína pero ayudan a presentar el dominio LRR adyacente para este propósito. Estos dominios pertenecen a la familia de dominios de tipo Ig en el sentido de que consisten en dos hojas beta intercaladas que siguen la conectividad clásica de los dominios de Ig. Sin embargo, las hebras beta en una de las hojas son mucho más pequeñas que en la mayoría de los dominios estándar similares a Ig, lo que la convierte en algo atípico.
Un grupo de azufre de hierro se encuentra en el N-terminal de algunas proteínas que contienen el dominio variante de repetición rico en leucina (LRV). Estas proteínas tienen una estructura de dos dominios, compuesta por un pequeño dominio N-terminal que contiene un grupo de cuatro residuos de cisteína que alberga el grupo 4Fe: 4S , y un dominio C-terminal más grande que contiene las repeticiones de LRV. Los estudios bioquímicos revelaron que el grupo 4Fe: 4S es sensible al oxígeno , pero no parece tener actividad redox reversible .
Ver también
Referencias
Otras lecturas
- Demasiado, John; Brändén, Carl-Ivar (1999). Introducción a la estructura de las proteínas (2ª ed.). Nueva York: Garland Publishing. ISBN 0-8153-2305-0.
- Wei T, Gong J, Jamitzky F, Heckl WM, Stark RW, Roessle SC (noviembre de 2008). "LRRML: una base de datos conformacional y una descripción XML de repeticiones ricas en leucina (LRR)" . BMC Struct. Biol . 8 (1): 47. doi : 10.1186 / 1472-6807-8-47 . PMC 2645405 . PMID 18986514 .
