Enfoque de genotipo primero - Genotype-first approach
El enfoque del primer genotipo es un tipo de estrategia que se utiliza en estudios epidemiológicos genéticos para asociar genotipos específicos con fenotipos clínicos aparentes de una enfermedad o rasgo complejo. A diferencia del “fenotipo primero”, la estrategia tradicional que ha estado guiando los estudios de asociación de todo el genoma (GWAS) hasta ahora, este enfoque caracteriza a los individuos primero por un genotipo estadísticamente común basado en pruebas moleculares antes de la clasificación fenotípica clínica. Este método de agrupación conduce a evaluaciones de pacientes basadas en una etiología genética compartida para los fenotipos observados, independientemente de su diagnóstico sospechoso. Por lo tanto, este enfoque puede prevenir el sesgo fenotípico inicial y permitir la identificación de genes que representan una contribución significativa a la etiología de la enfermedad .
Este enfoque no se ve afectado por la heterogeneidad fenotípica, la penetrancia incompleta y los niveles de expresividad. Por tanto, es útil en enfermedades complejas que también se solapan, como el trastorno del espectro autista y la discapacidad intelectual , lo que permite distinguir las enfermedades y determinar subtipos específicos de la enfermedad en función del contenido genómico .
Actualmente, el enfoque de genotipo primero se utiliza principalmente para objetivos de investigación. Sin embargo, las implicaciones de estos estudios pueden tener aplicaciones clínicas valiosas, que incluyen un mejor diagnóstico, asesoramiento y grupos de apoyo para personas con la misma etiología genética.
Fondo
Inicialmente, la idea de identificar el genotipo de los individuos y posteriormente su (s) fenotipo (s) asociado (s) se utilizó por primera vez en los primeros estudios citogenéticos . Alrededor de 1960, el descubrimiento de la trisomía 21 llevó a la comprensión de que la genética podría usarse para predecir fenotipos. Desde la década de 1960 hasta la de 1990, se utilizaron técnicas citogenéticas, como las bandas cromosómicas y la hibridación in situ por fluorescencia (FISH) para identificar y caracterizar fenotípicamente a los pacientes con anomalías cromosómicas.
Las enfermedades y los rasgos complejos plantean muchas dificultades para los estudios epidemiológicos debido a su naturaleza de enfermedades multifactoriales. Más de un gen puede ser la base de una enfermedad compleja y generalmente contribuye con un efecto menor que el observado en las enfermedades monogénicas ( enfermedades mendelianas ). Además, muchas de estas enfermedades complejas exhiben fenotipos diversos, así como una amplia gama de expresividad y penetrancia. Los genes también pueden ser pleiotrópicos , lo que explica muchos fenotipos clínicos aparentemente distintos. Estas características limitan la capacidad tanto de la investigación como de los estudios clínicos para designar genes o variantes causales de los fenotipos observados y clasificar los trastornos.
Los médicos están comenzando a reconocer la necesidad de clasificar las enfermedades genómicas por un genotipo común en lugar de un fenotipo común y cómo el enfoque del genotipo primero puede beneficiar este propósito.
Métodos
Se pueden usar varios métodos con un enfoque de genotipo primero, sin embargo, generalmente se incluyen los siguientes pasos:
- Establecimiento de una población de estudio y genotipado
- Análisis de variantes genómicas de interés encontradas en la población de estudio
- Las poblaciones de estudio se ensamblan según el genotipo
- Asociación de genotipo a fenotipo (s) dentro del grupo respectivo
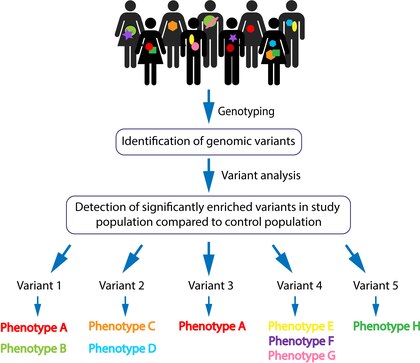
La genotipificación se genera utilizando tecnologías de secuenciación de próxima generación (incluida la secuenciación del genoma completo y la secuenciación del exoma ) y análisis de microarrays . Luego, los datos brutos se analizan estadísticamente para determinar la frecuencia poblacional de las variantes. Las variantes comunes se filtran y la patogenicidad se determina a través de las implicaciones genéticas predichas. Estos pasos permiten la identificación de supuestas variantes altamente penetrantes y su locus específico . Las variantes seleccionadas generalmente se vuelven a secuenciar para su validación (mediante secuenciación de Sanger dirigida ). Las variantes genómicas validadas se pueden analizar para detectar recurrencias entre los individuos afectados dentro de la cohorte. La patogenicidad de una variante genómica se basa estadísticamente en su presencia significativamente abundante en los individuos afectados en comparación con los no afectados, no exclusivamente en la nocividad de la variante. Entonces, una variante candidata puede asociarse con un fenotipo compartido con la aspiración de que a medida que se identifiquen más pacientes que muestren la misma variante con el mismo fenotipo, se pueda establecer una asociación más fuerte. Por último, se hace una delimitación entre una variante específica y los fenotipos clínicos asociados [Figura 1].
Implicaciones clínicas y ejemplos
El enfoque de genotipo primero se ha utilizado para diagnosticar a pacientes con enfermedades raras, identificar nuevas asociaciones entre el genotipo y el fenotipo de la enfermedad y caracterizar enfermedades poco comunes o heterogéneas según el genotipo del paciente. En 2014, se utilizó el enfoque de genotipo primero para evaluar variantes raras y de baja frecuencia en la población finlandesa. Dado que la población finlandesa está aislada y ha sufrido recientemente un cuello de botella en la población, en comparación con otros países, ofrece dos beneficios principales para los estudios de genotipo primero. Las variantes deletéreas se encuentran en frecuencias más altas dentro de un espectro más pequeño de variantes raras en poblaciones fundadoras con cuello de botella. Al comparar las variantes encontradas usando la secuenciación del exoma completo (WES) en la población finlandesa con WES de un grupo de control de europeos no finlandeses, se observaron variantes de pérdida de función (LOF) con mayor frecuencia en la población finlandesa. A continuación, se analizaron los fenotipos de los individuos finlandeses con estas variantes de LOF para determinar nuevas asociaciones genotipo-fenotipo. Estas asociaciones detectadas incluyeron una que podría ser letal para el embrión, información que podría no haber sido descubierta en la investigación utilizando un enfoque de fenotipo primero. Además, los investigadores también descubrieron nuevas variantes de empalme en el gen LPA que reducen los niveles de apolipoproteína A y ofrecen un fenotipo protector contra las enfermedades cardiovasculares.
La evaluación del genotipo primero se está convirtiendo en el enfoque estándar para el diagnóstico clínico de enfermedades complejas heterogéneas. Los síndromes de microduplicación y microdeleción tienen una variedad de características, incluida la discapacidad intelectual y el retraso del desarrollo , que varían en gravedad, lo que hace que los pacientes con estos síndromes sean muy difíciles de diagnosticar. Desde el desarrollo de las tecnologías de secuenciación de próxima generación, los médicos han podido utilizar un enfoque de genotipo primero para agrupar a estos pacientes en función de su microdeleción o duplicación y documentar las características de la enfermedad presentes en estos grupos. El análisis de micromatrices cromosómicas, en particular, se está utilizando clínicamente para ayudar en el diagnóstico de pacientes con síndromes de microdeleción y microduplicación. En enfermedades, como el trastorno del espectro autista (TEA), donde diferenciar a los pacientes en grupos de subtipos de enfermedades según el fenotipo es un desafío, los estudios de genotipo primero permiten clasificar a los pacientes en subtipos según su genética. Esto, a su vez, proporcionará una mayor comprensión de las causas genéticas de los TEA y, en el futuro, podría definir subtipos específicos de TEA para los pacientes a los que se les diagnosticará.
La investigación del genotipo primero, a través de la identificación de nuevos genes asociados a enfermedades, también puede beneficiar a las compañías farmacéuticas y al desarrollo de fármacos. En el caso de enfermedades complejas, el uso de la primera asociación genética del fenotipo, el desarrollo de terapias a menudo no tiene éxito debido a que múltiples genes contribuyen a una enfermedad. Con las asociaciones de genotipo primero, primero se identifica el objetivo terapéutico potencial.
Ventajas y limitaciones
Ventajas
- Un cambio hacia la caracterización de los individuos por un genotipo común en lugar de la presentación clínica permitirá clasificar nuevos síndromes y la clasificación genética de ciertos subtipos de enfermedades, a medida que la secuenciación se vuelva más barata, más rápida y más eficiente.
- La herencia de una variante genómica de un padre sano no daría lugar a su exclusión del análisis de variantes, lo que explica el papel de los modificadores en el resultado fenotípico.
- Este enfoque no se ve afectado por la heterogeneidad fenotípica, la penetrancia incompleta y la expresividad.
- Este enfoque contribuye al estudio de la expresividad, la pleiotropía y las mutaciones esporádicas.
- Este enfoque examina las mutaciones altamente penetrantes que están asociadas con la enfermedad independientemente de los antecedentes genéticos.
- El fenotipado completo y detallado es posible incluso con un pequeño número de pacientes con etiología genética común.
- Este enfoque puede identificar presentaciones atípicas de la enfermedad cuando se usa con fines diagnósticos.
Limitaciones
- El fenotipo puede cambiar con el tiempo (por ejemplo, se vuelve más severo, cambio en la ubicación física) haciendo que los estudios de genotipo primero sean una suposición sobre el papel de la variante en la manifestación de la enfermedad en un momento específico. Por tanto, el seguimiento longitudinal es importante para que la asociación genotipo-fenotipo se valore con el tiempo y examine el pronóstico de la enfermedad.
- Las variantes identificadas que podrían contribuir a un fenotipo leve, o a una variedad de fenotipos, no serían beneficiosas para determinar el diagnóstico y el pronóstico. Sin embargo, en el futuro, a medida que se clasifiquen más subtipos de enfermedades, los fenotipos leves podrían tener más relevancia.
- La asociación genotipo-fenotipo se basa en la presentación de fenotipos clínicamente reconocibles.
- Como se vio en otros estudios de asociación del genoma, este enfoque puede generar variantes de importancia desconocida , especialmente cuando se utiliza para el diagnóstico.
Ver también
- Enfermedad compleja
- Estudio de asociación de genoma completo (GWAS)
- Microarray
- Secuenciación del exoma completo (WES)
- Secuenciación del genoma completo (WGS)