Nitrato de flúor - Fluorine nitrate

|
|
|
|
| Identificadores | |
|---|---|
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| F N O 3 | |
| Masa molar | 81,002 g · mol −1 |
| Densidad | 2.217 g / L |
| Punto de fusion | −175 ° C (−283,0 ° F; 98,1 K) |
| Punto de ebullición | −46 ° C (−51 ° F; 227 K) |
| Termoquímica | |
| +10,46 kJ / mol | |
| Riesgos | |
| Principales peligros | Gas explosivo |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
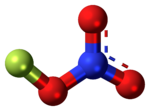
El nitrato de flúor es un derivado inestable del ácido nítrico con la fórmula FNO
3. Es sensible a los golpes. Debido a su inestabilidad, a menudo se produce a partir de nitrato de cloro según sea necesario.
Síntesis y propiedades
El nitrato de flúor se forma cuando se burbujea gas flúor a través de ácido nítrico o se hace reaccionar con nitrato de potasio sólido :
- F
2 + HNO
3 → FNO
3 + HF
- F
2 + KNO
3 → FNO
3 + KF
Se descompone en agua para formar oxígeno gaseoso, difluoruro de oxígeno , ácido fluorhídrico y ácido nítrico.
Referencias
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química de los Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
Sales y derivados covalentes del ion nitrato
| Este artículo relacionado con un compuesto inorgánico es un trozo . Puedes ayudar a Wikipedia expandiéndolo . |
