Ácido cloroso - Chlorous acid
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Ácido cloroso
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| H Cl O 2 | |
| Masa molar | 68,46 g / mol |
| Acidez (p K a ) | 1,96 |
| Base conjugada | Clorita |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
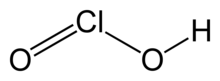
El ácido cloroso es un compuesto inorgánico con la fórmula HClO 2 . Es un ácido débil . El cloro tiene un estado de oxidación +3 en este ácido. La sustancia pura es inestable, desproporcionada en ácido hipocloroso (estado de oxidación de Cl +1) y ácido clorhídrico (estado de oxidación de Cl +5):
- 2 HClO 2 → HClO + HClO 3
Aunque el ácido es difícil de obtener en sustancia pura, la base conjugada, clorito , derivada de este ácido es estable. Un ejemplo de una sal de este anión es el conocido clorito de sodio . Esta y otras sales relacionadas se utilizan a veces en la producción de dióxido de cloro .
Preparación
El HClO 2 se puede preparar mediante la reacción de bario o clorito de plomo y ácido sulfúrico diluido :
- Ba (ClO 2 ) 2 + H 2 SO 4 → BaSO 4 + 2 HClO 2
- Pb (ClO 2 ) 2 + H 2 SO 4 → PbSO 4 + 2 HClO 2
Estabilidad
El ácido cloroso es un potente agente oxidante, aunque su tendencia a la desproporción contrarresta su potencial oxidante.
El cloro es el único halógeno que forma un ácido aislable de fórmula HXO 2 . Ni ácido bromoso ni ácido iodous nunca ha sido aislado. Se conocen algunas sales de ácido bromoso , bromitos, pero no yoditos .
Referencias
![]() Medios relacionados con el ácido cloroso en Wikimedia Commons
Medios relacionados con el ácido cloroso en Wikimedia Commons
- ^ a b Egon Wiberg, Arnold Frederick Holleman (2001) Química inorgánica , Elsevier ISBN 0-12-352651-5
| Este artículo relacionado con un compuesto inorgánico es un trozo . Puedes ayudar a Wikipedia expandiéndolo . |
