Enlace carbono-carbono - Carbon–carbon bond
Un enlace carbono-carbono es un enlace covalente entre dos átomos de carbono . La forma más común es el enlace simple : un enlace compuesto por dos electrones , uno de cada uno de los dos átomos. El enlace sencillo carbono-carbono es un enlace sigma y se forma entre un orbital hibridado de cada uno de los átomos de carbono. En etano , los orbitales sp son 3 - hibridado orbitales, pero enlaces simples formadas entre átomos de carbono con otras hibridaciones no ocurrir (por ejemplo sp 2 a SP 2 ). De hecho, los átomos de carbono en el enlace sencillo no necesitan tener la misma hibridación. Los átomos de carbono también pueden formar dobles enlaces en compuestos llamados alquenos o triples enlaces en compuestos llamados alquinos . Se forma un doble enlace con un orbital hibridado con sp 2 y un orbital p que no está involucrado en la hibridación. Se forma un triple enlace con un orbital con hibridación sp y dos orbitales p de cada átomo. El uso de orbitales p forma un enlace pi .
Cadenas y ramificaciones
El carbono es uno de los pocos elementos que puede formar largas cadenas de sus propios átomos, una propiedad llamada catenation . Esto unido a la fuerza del enlace carbono-carbono da lugar a una enorme cantidad de formas moleculares, muchas de las cuales son elementos estructurales importantes de la vida, por lo que los compuestos de carbono tienen su propio campo de estudio: la química orgánica .
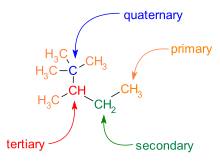
La ramificación también es común en los esqueletos C-C. Los átomos de carbono de una molécula se clasifican según el número de vecinos de carbono que tienen:
- Un carbono primario tiene un vecino de carbono.
- Un carbono secundario tiene dos vecinos de carbono.
- Un carbono terciario tiene tres vecinos de carbono.
- Un carbono cuaternario tiene cuatro vecinos de carbono.
En las "moléculas orgánicas estructuralmente complejas", es la orientación tridimensional de los enlaces carbono-carbono en los loci cuaternarios la que dicta la forma de la molécula. Además, los loci cuaternarios se encuentran en muchas moléculas pequeñas biológicamente activas, como la cortisona y la morfina .
Síntesis
Las reacciones de formación de enlaces carbono-carbono son reacciones orgánicas en las que se forma un nuevo enlace carbono-carbono. Son importantes en la producción de muchos productos químicos artificiales, como productos farmacéuticos y plásticos .
Algunos ejemplos de reacciones que forman enlaces carbono-carbono son las reacciones aldólicas , las reacciones de Diels-Alder , la adición de un reactivo de Grignard a un grupo carbonilo , una reacción de Heck , una reacción de Michael y una reacción de Wittig .
La síntesis dirigida de estructuras tridimensionales deseadas para carbonos terciarios fue resuelto en gran parte durante la tarde 20 º siglo, pero la misma capacidad de síntesis de carbono cuaternario directa no comenzó a emerger hasta la primera década del 21 st siglo.
Fortalezas y longitudes de la unión
El enlace simple carbono-carbono es más débil que los enlaces CH, OH, NH, HH, H-Cl, CF y muchos dobles o triples, y es comparable en fuerza a los enlaces CO, Si-O, PO y SH, pero comúnmente es considerado como fuerte.
| Enlace C – C | Molécula | Energía de disociación del enlace (kcal / mol) |
|---|---|---|
| CH 3 −CH 3 | etano | 90 |
| C 6 H 5 −CH 3 | tolueno | 102 |
| C 6 H 5 −C 6 H 5 | bifenilo | 114 |
| CH 3 C (O) −CH 3 | acetona | 84 |
| CH 3 −CN | acetonitrilo | 136 |
| CH 3 −CH 2 OH | etanol | 88 |
Los valores dados anteriormente representan las energías de disociación del enlace CC que se encuentran comúnmente; ocasionalmente, los valores atípicos pueden desviarse drásticamente de este rango.
| Molécula | Etano | Etileno | Acetileno |
|---|---|---|---|
| Fórmula | C 2 H 6 | C 2 H 4 | C 2 H 2 |
| Clase | alcano | alqueno | alquino |
| Estructura |

|

|

|
| Hibridación de carbono | sp 3 | sp 2 | sp |
| Longitud del enlace CC | 1,535 Å | 1,339 Å | 1,203 Å |
| Proporción de enlace simple CC | 100% | 87% | 78% |
| Método de determinación de estructura | espectroscopia de microondas | espectroscopia de microondas | espectroscopia infrarroja |
Casos extremos
Bonos simples CC largos y débiles
Se han identificado varios casos extremos en los que el enlace CC se alarga. En el dímero de Gomberg , un enlace CC es bastante largo a 159,7 picómetros . Es este enlace el que se rompe fácilmente y de manera reversible a temperatura ambiente en solución:
En la molécula aún más congestionada hexakis (3,5-di- terc- butilfenil) etano , la energía de disociación del enlace para formar el radical triarilmetilo estabilizado es sólo de 8 kcal / mol. También como consecuencia de su severa congestión estérica, el hexakis (3,5-di- terc- butilfenil) etano tiene un enlace central muy alargado con una longitud de 167 µm.
Dobles enlaces CC retorcidos y débiles
La estructura del tetrakis (dimetilamino) etileno (TDAE) está muy distorsionada. El ángulo diedro para los dos extremos de N 2 C es 28º aunque la distancia C = C es normal de 135 pm. El tetraisopropiletileno casi isoestructural también tiene una distancia C = C de 135 pm, pero su núcleo C 6 es plano.
Triples enlaces CC cortos y fuertes
En el extremo opuesto, el enlace sencillo carbono-carbono central del diacetileno es muy fuerte a 160 kcal / mol, ya que el enlace sencillo une dos carbonos de hibridación sp. Los enlaces múltiples carbono-carbono son generalmente más fuertes; Se ha determinado que el doble enlace de etileno y el triple enlace de acetileno tienen energías de disociación de enlaces de 174 y 230 kcal / mol, respectivamente. Se ha observado un enlace triple muy corto de 115 pm para la especie de yodonio [HC≡C – I + Ph] [CF 3 SO 3 - ], debido a la fracción de yodonio fuertemente atrayente de electrones.