Ácido arsénico - Arsenic acid
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Ácido arsénico, ácido arsórico
|
|
| Otros nombres
Ácido arsénico Ácido
ortoarsénico Desecante L-10 Zotox |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.029.001 |
| Número CE | |
| KEGG | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 1553, 1554 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| H 3 AsO 4 | |
| Masa molar | 141,94 g / mol |
| Apariencia | Cristales blancos translúcidos, higroscópicos . |
| Densidad | 2,5 g / cm 3 |
| Punto de fusion | 35,5 ° C (95,9 ° F; 308,6 K) |
| Punto de ebullición | 120 ° C (248 ° F; 393 K) se descompone |
| 16,7 g / 100 ml | |
| Solubilidad | soluble en alcohol |
| Presión de vapor | 55 hPa (50 ° C) |
| Acidez (p K a ) | 2,19, 6,94, 11,5 |
| Base conjugada | Arsenato |
| Estructura | |
| Tetraédrico | |
| Riesgos | |
| Principales peligros | Extremadamente tóxico, cancerígeno, corrosivo. |
| Pictogramas GHS |
    
|
| Palabra de señal GHS | Peligro |
| H301 , H312 , H314 , H318 , H331 , H350 , H361 , H400 , H410 | |
| P201 , P202 , P260 , P261 , P264 , P270 , P271 , P273 , P280 , P281 , P301 + 310 , P301 + 330 + 331 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P308 + 313 , P310 , P311 , P312 , P321 , P322 , P330 , P363 , P391 | |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | No es inflamable |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis media )
|
48 mg / kg (rata, oral)
6 mg / kg (conejo, oral) |
| Compuestos relacionados | |
|
Otros aniones
|
Ácido fosfórico |
|
Otros cationes
|
Arseniato de sodio |
|
Compuestos relacionados
|
Ácido arsénico Pentóxido de arsénico |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |

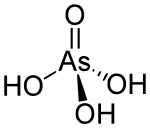
El ácido arsénico es el compuesto químico con la fórmula H 3 AsO 4 . Escrito de forma más descriptiva como AsO (OH) 3 , este ácido incoloro es el análogo de arsénico del ácido fosfórico . Las sales de arsenato y fosfato se comportan de manera muy similar. El ácido arsénico como tal no se ha aislado, sino que solo se encuentra en solución, donde está en gran parte ionizado. Su forma hemihidrato (H 3 AsO 4 ·1/2H 2 O) forma cristales estables. Las muestras cristalinas se deshidratan con condensación a 100 ° C.
Propiedades
Es una especie tetraédrica de simetría idealizada C 3v con longitudes de enlace As – O que van de 1,66 a 1,71 Å.
Al ser un ácido triprótico , su acidez se describe mediante tres equilibrios:
- H 3 AsO 4 + H 2 O ⇌ H
2AsO-
4 + H 3 O + (p K a1 = 2,19) -
H
2AsO-
4 + H 2 O ⇌ HAsO2−
4 + H 3 O + (p K a2 = 6,94) -
HAsO2−
4 + H 2 O ⇌ AsO3−
4 + H 3 O + (p K a3 = 11,5)
Estos valores de p K a son cercanos a los del ácido fosfórico . El ion arseniato altamente básico ( AsO3−
4) es el producto de la tercera ionización. A diferencia del ácido fosfórico, el ácido arsénico es un oxidante, como lo ilustra su capacidad para convertir el yoduro en yodo .
Preparación
El ácido arsénico se prepara tratando trióxido de arsénico con ácido nítrico concentrado . El trióxido de dinitrógeno se produce como subproducto.
- Como 2 O 3 + 2 HNO 3 + 2 H 2 O → 2 H 3 AsO 4 + N 2 O 3
La solución resultante se enfría para dar cristales incoloros del hemihidrato H 3 AsO 4 .1/2H 2 O, aunque el dihidrato H 3 AsO 4 · 2H 2 O se produce cuando la cristalización se produce a temperaturas más bajas.
Otros metodos
El ácido arsénico se forma lentamente cuando el pentóxido de arsénico se disuelve en agua y cuando el ácido meta o piroarsénico se trata con agua fría. El ácido arsénico también se puede preparar directamente a partir de arsénico elemental humedeciéndolo y tratándolo con ozono .
- 2 As + 3 H 2 O + 5 O 3 → 2 H 3 AsO 4 + 5 O 2
Aplicaciones
Las aplicaciones comerciales del ácido arsénico están limitadas por su toxicidad. Es un precursor de una variedad de pesticidas. Ha encontrado un uso ocasional como conservante de la madera , biocida de amplio espectro , agente de acabado para vidrio y metal, y reactivo en la síntesis de algunos colorantes y compuestos orgánicos de arsénico.
La seguridad
El ácido arsénico es extremadamente tóxico y cancerígeno, como todos los compuestos de arsénico. También es corrosivo . La DL 50 en conejos es de 6 mg / kg (0,006 g / kg).

