Tribromuro de antimonio - Antimony tribromide
|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
tribromostibane
|
|
| Otros nombres
Bromuro de antimonio (III)
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.029.254 |
| Número CE | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 1549 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| SbBr 3 | |
| Masa molar | 361,472 g / mol |
| Apariencia | cristales incoloros a amarillos higroscópicos |
| Densidad | 4,35 g / cm 3 |
| Punto de fusion | 96,6 ° C (205,9 ° F; 369,8 K) |
| Punto de ebullición | 288 ° C (550 ° F; 561 K) |
| hidrólisis parcial soluble | |
| Solubilidad | soluble en HCl diluido , HBr , CS 2 , acetona , benceno , cloroformo , amoníaco , alcohol |
| -115,0 · 10 −6 cm 3 / mol | |
|
Índice de refracción ( n D )
|
1,74 |
| 2,47 D | |
| Estructura | |
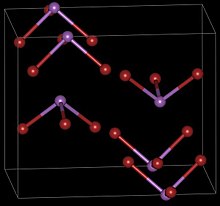
| Ortorrómbico , oP16 , SpaceGroup = Pnma, No. 62 (forma β) | |
| Termoquímica | |
|
Capacidad calorífica ( C )
|
96 J / mol K |
| -259 kJ / mol | |
| Peligros | |
| Pictogramas GHS |
 
|
| Palabra de señal GHS | Advertencia |
| H302 , H332 , H411 | |
| P261 , P264 , P270 , P271 , P273 , P301 + 312 , P304 + 312 , P304 + 340 , P312 , P330 , P391 , P501 | |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis mediana )
|
7000 mg / kg |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
TWA 0,5 mg / m 3 (como Sb) |
|
REL (recomendado)
|
TWA 0,5 mg / m 3 (como Sb) |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El tribromuro de antimonio ( Sb Br 3 ) es un compuesto químico que contiene antimonio en su estado de oxidación +3.
Producción
Puede prepararse mediante la reacción de antimonio con bromo elemental o mediante la reacción de trióxido de antimonio con ácido bromhídrico .
Alternativamente, se puede preparar mediante la acción del bromo sobre una mezcla de sulfuro de antimonio y trióxido de antimonio a 250 ° C.
Usos
Se puede agregar a polímeros como el polietileno como retardante de fuego . También se utiliza en la producción de otros compuestos de antimonio, en análisis químicos, como mordiente y en teñido.
Propiedades químicas
El tribromuro de antimonio tiene dos formas cristalinas, ambas con simetrías ortorrómbicas . Cuando una solución de disulfuro de carbono caliente de SbBr 3 se enfría rápidamente, cristaliza en α-SbBr 3 en forma de aguja , que luego se convierte lentamente en la forma β más estable.
El tribromuro de antimonio se hidroliza en agua para formar ácido bromhídrico y trióxido de antimonio:
- 2 SbBr 3 + 3 H 2 O → Sb 2 O 3 + 6 HBr
Referencias
- ^ a b Guía de bolsillo de NIOSH sobre peligros químicos. "# 0036" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Yang, YP; DG Brewer; JES Venart (1991). "Un estudio de la acción sinérgica del óxido de antimonio en el polietileno ignífugo". Fuego y Materiales . 15 : 37–42. doi : 10.1002 / fam.810150107 .
- ^ "Tribromuro de antimonio" http://cameochemicals.noaa.gov/chemical/2501
- ^ Okuda, Tsutomu; Terao, Hiromitsu; Ege, Osamu; Negita, Hisao (1970). "Estudios estructurales del tribromuro de antimonio y su complejo molecular con benceno mediante la resonancia cuadrupolo nuclear 81Br" . Boletín de la Sociedad Química de Japón . 43 (8): 2398. doi : 10.1246 / bcsj.43.2398 .
