Alameticina - Alamethicin

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
N -acetil-2-methylalanyl- L prolil-2-methylalanyl- L alanil-2-methylalanyl- L -alanyl- L -glutaminyl-2-methylalanyl- L valil-2-methylalanylglycyl- L leucil-2- methylalanyl- L prolil- L valil-2-metilalanilo-2-methylalanyl- L -α-glutamil N 1 - [(1 S ) -1-bencil-2-hidroxietil] - L -glutamamide
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.121.626 |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 92 H 150 N 22 O 25 | |
| Masa molar | 1964,31 g / mol |
| Apariencia | Sólido blanquecino |
| Punto de fusion | 255 a 270 ° C (491 a 518 ° F; 528 a 543 K) |
| Insoluble | |
| Solubilidad en DMSO , metanol , etanol | Soluble |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
La alameticina es un antibiótico peptídico formador de canales , producido por el hongo Trichoderma viride . Pertenece a los péptidos de peptaibol que contienen el residuo de aminoácido no proteinogénico Aib ( ácido 2-aminoisobutírico ). Este residuo induce fuertemente la formación de estructura alfa-helicoidal . La secuencia de péptidos es:
Ac-Aib-Pro-Aib-Ala-Aib-Ala-Gln-Aib-Val-Aib-Gly-Leu-Aib-Pro-Val-Aib-Aib-Glu-Gln-Phl
(Ac = acetilo, Phl = fenilalaninol , Aib = ácido 2-aminoisobutírico )
En las membranas celulares , se forma de voltaje dependientes de iones de canales por agregación de cuatro a seis moléculas .
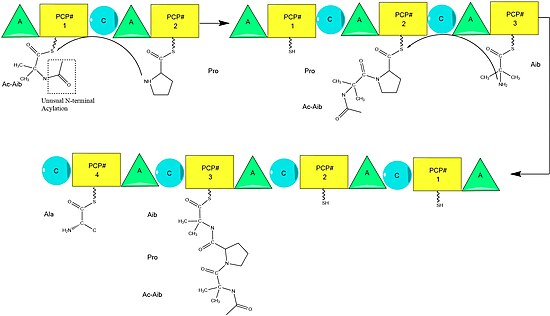
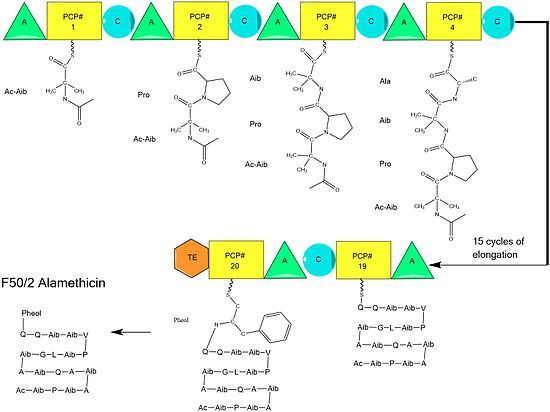
Biosíntesis
Se plantea la hipótesis de que la biosíntesis de alameticina está catalizada por alameticina sintasa, una péptido sintasa no ribosomal (NRPS) aislada por primera vez en 1975. Aunque hay varias secuencias aceptadas del péptido de alameticina, la evidencia sugiere que todas siguen el mecanismo general de NRPS con pequeñas variaciones en aminoácidos seleccionados . Comenzando con la acilación del N terminal del primer ácido aminoisobutírico en la enzima ALM sintasa por Acetil-CoA , esto es seguido por la condensación secuencial de aminoácidos por cada unidad modular de la sintetasa. Los aminoácidos se adenilan inicialmente mediante un dominio de " adenilación " (A) antes de unirse mediante un enlace tioéster a una proteína transportadora de peptidilo similar a la proteína transportadora de acilo . La cadena en crecimiento se une al aminoácido que lleva PCP por el dominio de "condensación" (C), seguido de otra ronda de las mismas reacciones por el siguiente módulo.
El ensamblaje se completa con la adición de fenilalaninol, un inusual sustrato similar a un aminoácido. Después de la adición de fenilalaninol, la cadena peptídica completa es escindida por el dominio tioesterasa, escindiendo el enlace tioéster y dejando un alcohol.
Referencias
Otras lecturas
- Jones, LR; Maddock, SW; Besch, HR Jr (1980). "Efecto desenmascarador de alameticina sobre la (Na +, K +) - ATPasa, adenilato ciclasa acoplada al receptor beta-adrenérgico y actividades de proteína quinasa dependientes de AMPc de vesículas sarcolemáticas cardíacas" . J. Biol. Chem . 255 (20): 9971–9980. doi : 10.1016 / S0021-9258 (18) 43488-6 . PMID 6253461 .
- Explore las estructuras de alameticina en el banco de datos de proteínas
-
Alamethicin en Norine
- A partir de "Un modelo de canal iónico dependiente de voltaje inferido de la estructura cristalina de alameticina a una resolución de 1,5 A". Fox Jr., RO; Richards, FM (1982). "Un modelo de canal iónico dependiente de voltaje inferido de la estructura cristalina de alameticina a una resolución de 1,5 A". Naturaleza . 300 (5890): 325-30. Código Bibliográfico : 1982Natur.300..325F . doi : 10.1038 / 300325a0 . PMID 6292726 . S2CID 4278453 .
- Leitgeb, Balázs; Szekeres, András; Manczinger, László; Vágvölgyi, Csaba; Kredics, László (1 de junio de 2007). "La historia de la alameticina: una revisión del Peptaibol más ampliamente estudiado". Química y Biodiversidad . 4 (6): 1027–1051. doi : 10.1002 / cbdv.200790095 . ISSN 1612-1880 . PMID 17589875 . S2CID 40886688 .